Wie das Licht der Sonne
Anzeigen
Leuchtdioden liefern sehr energieeffizientes Licht. Könnte man sie zur Beleuchtung einsetzen, würde das eine Menge Energie sparen. Bisher gelingt es zwar, rote und blaue LEDs herzustellen, doch fehlen derzeit noch grüne LEDs, um das Spektrum des Tageslichts nachzuempfinden und damit weißes Licht zu erzeugen. Zinkoxid könnte diese Lücke schließen.

Frisch aus der Schmelze erstarrte Zinkoxid-Kristalle schimmern rot, weil sie noch atomare Defekte enthalten. Ein nachfolgendes Tempern - Erhitzen auf ca. 1.000 °C - bringt die Defekte zum Verschwinden und liefert ein blassgelbes Material, das zu Halbleiter-Wafern verarbeitet wird.
IKZ
Die Zeiten, in denen Fahrradfahrer nachts mit ihrem schwachen dynamobetriebenen Licht leicht zu übersehen waren, sind vorbei. Heutzutage blinkt und leuchtet es einem schon von weitem entgegen. Das weiße Vorderlicht ist dabei besonders grell, es erscheint eher blau als weiß. Das Wohnzimmer möchte sich mit diesem Licht wohl niemand beleuchten.
Das Licht der Sonne setzt sich aus rotem, grünem und blauem Licht zusammen - mit sämtlichen Zwischentönen. Grün ist in dem Spektrum am meisten vertreten. Bisher wird zur Herstellung von Leuchtdioden Galliumarsenid (GaAs) für rotes Licht und Galliumnitrid (GaN) für blaues Licht verwendet. Diese beiden Halbleitermaterialien bilden auch die Grundlage für Fahrradlampen. Da das grüne Lichtspektrum fehlt, empfinden wir das Licht als kalt und unnatürlich. Dr. Detlef Klimm und seine Mitarbeiter vom Leibniz-Institut für Kristallzüchtung (IKZ)entwickeln derzeit ein Material, das für Leuchtdioden mit allen sichtbaren Wellenlängen geeignet ist. Die Physiker nennen solche Materialien breitbandige Halbleiter.
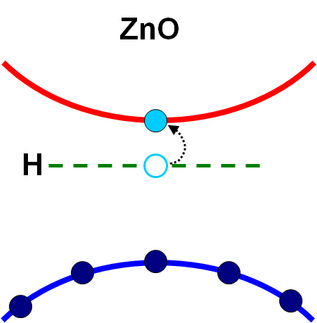
Ein solch breitbandiger Halbleiter ist das Zinkoxid (ZnO). Es hat eine relativ einfache Kristallstruktur und eignet sich daher gut für den Bau von Leuchtdioden. Die Schwierigkeit besteht darin, einen reinen Zinkoxid-Kristall herzustellen. Zinkoxid liegt gewöhnlich als weißes Pulver vor, es ist zum Beispiel in Salben zur Wundheilung enthalten. Normalerweise gehen die Wissenschaftler zur Herstellung eines Kristalls so vor: In einem Tiegel schmelzen sie das Material. Damit sich während des Abkühlens beim Übergang von der flüssigen zur festen Phase die gewünschte Kristallstruktur bildet, befindet sich am Boden des Topfes schon ein kleiner fertiger Kristall, der "Keim", an dessen Gitterstruktur die Moleküle beim Abkühlen andocken. So setzt sich die Struktur immer weiter fort.
Beim Zinkoxid funktioniert das nicht so einfach, da es beim Erhitzen direkt verdampft, ohne vorher flüssig zu werden. Doch Detlef Klimm weiß dafür eine Lösung: "Ein leichter Überdruck reicht, damit es beim Erhitzen von Zinkoxid einen flüssigen Zustand gibt." Der Schmelzpunkt liegt bei fast 2.000 Grad Celsius. Daraus ergibt sich ein weiteres, etwas kniffligeres Problem: Der Schmelztiegel darf auch bei großer Hitze nicht selber schmelzen, und er darf nicht mit dem Material reagieren, denn sonst ist der Kristall nicht rein. Ein gutes Tiegelmaterial ist Iridium. Es ist hitzebeständig und chemisch stabil. Allerdings reagiert Iridium leicht mit Sauerstoff. Sauerstoff liegt zwar eigentlich gar nicht vor, doch zerfällt das Zinkoxid beim Erhitzen leicht in Zink und Sauerstoff, und reagiert wieder zu Zinkoxid. Ein solches Hin- und Herschaukeln nennen die Chemiker Gleichgewichtsreaktion. "Bei hohen Temperaturen macht das nichts aus", erläutert Klimm. "Das Iridium oxidiert nur bei niedrigen Temperaturen. Doch da müssen wir eben durch." Klimms Idee zur Lösung des Problems ist so genial wie einfach: Wenn die Umgebung bei hohen Temperaturen mit Sauerstoff übersättigt wäre, würde das Zinkoxid nicht mehr so leicht zerfallen. Bei tieferen Temperaturen darf hingegen kein Sauerstoff vorhanden sein, denn sonst würde er den Iridium-Tiegel verbrennen. Also hat Klimm als Atmosphäre Kohlendioxid in den Tiegel gegeben, das dieselbe Gleichgewichtsreaktion wie das Zinkoxid aufweist. Im Laufe der Erhitzung zerfällt das Kohlendioxid in CO und Sauerstoff, in der Atmosphäre ist dann viel Sauerstoff enthalten, und der Zerfall des Zinkoxids wird gehemmt. Beim Abkühlen wird überschüssiger Sauerstoff wieder durch das CO gebunden und somit das Verbrennen des Iridiums verhindert. So kann ein reiner Kristall entstehen, den kein Iridium "verschmutzt".
Klimm hat in Versuchen gezeigt, dass das Prinzip funktioniert und hat ein Patent darauf. Nun geht es darum, noch weiter zu tüfteln und das Verfahren zu optimieren. Derzeit wird eine neue Anlage in Betrieb genommen, in der es nur minimale Temperaturschwankungen gibt, so dass keine Risse im Kristall entstehen. Das Verfahren ist aber schon so weit entwickelt, dass Klimm und seine Mitarbeiter mit der Berliner Firma CrysTec einen Industriepartner gefunden haben, der aus den im IKZ hergestellten Zinkoxid-Kristallen Wafer herstellt und kommerziell vertreibt. Nun wird noch ein Partner für den übernächsten Schritt gesucht, nämlich die Herstellung von Leuchtdioden aus Zinkoxid.