Einem alten Metall neue Tricks beibringen
Wissenschaftler haben einen Weg gefunden, ein in der Synthesechemie häufig verwendetes Reagenz zu recyceln
Anzeigen
Das metallische Element Samarium ist in Verbindung mit anderen Elementen ein unglaublich nützliches chemisches Reagenz für die Synthese von Molekülen, die zu neuen Arzneimitteln führen können. Das 1879 in einer russischen Mine entdeckte Element wurde nach dem Mineral benannt, in dem es gefunden wurde, dem Samarskit, der wiederum nach dem russischen Bergbauingenieur Vassili Samarsky-Bykhovets benannt wurde. Das gebräuchlichste Samarium-Reagenz ist Samariumdiiodid, das aus einem Samarium-Atom und zwei Atomen des Elements Jod besteht.

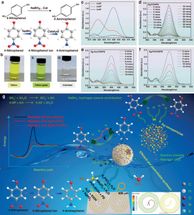
Dieses Bild zeigt die verschiedenen Stadien einer chemischen Reaktion mit dem Samariumdiiodid-Reagenz. Der Kolben auf der linken Seite enthält eine gelbe, inaktive Form der Verbindung - mit der Zeit wird die Verbindung aktiv und färbt sich violett, wie auf der rechten Seite zu sehen ist. Dieser Farbwechsel erfolgt, weil sich die Oxidationsstufe des Samarium-Reagens von 3+ zu 2+ oder von Sm(III) zu Sm(II) ändert, was bedeutet, dass es ein Elektron gewinnt.
Caltech/Chungkeun Shin
Die Vergrößerung dieses vielseitigen Reagenzes auf Mengen, die für den industriellen Einsatz ausreichen, hat sich jedoch als schwierig erwiesen. "Das Reagenz ist luftempfindlich, so dass man die Lösung oft direkt vor der Reaktion frisch ansetzen muss", sagt der Caltech-Diplomstudent Chungkeun Shin, der im Labor von Sarah Reisman, Bren-Professorin für Chemie und Norman Davidson-Lehrstuhlinhaberin der Caltech-Abteilung für Chemie und Chemieingenieurwesen, arbeitet. "Und wir müssen oft große Mengen davon verwenden, selbst bei kleinen Reaktionen, so dass es für die Durchführung von Reaktionen im industriellen Maßstab nicht praktisch ist.
Wie in der Ausgabe vom 23. August der Zeitschrift Science berichtet wird, ist es Caltech-Chemikern gelungen, dieses Rätsel der Skalierung zu lösen. Ihre Lösung ermöglicht es dem Samariumdiiodid-Reagenz, sich im Wesentlichen selbst zu recyceln und in einer einzigen Reaktion wiederholt zu verwenden, was bedeutet, dass keine großen Mengen an Lösungsmitteln und neuen Präparaten mehr benötigt werden.
"Samariumdiiodid wurde in der Wissenschaft für die Synthese von Naturstoffen wie Taxol, einem Krebsmittel, verwendet, aber das Reagenz ist für die Herstellung solcher Produkte im industriellen Maßstab nicht geeignet", sagt Reisman. "Der Durchbruch besteht darin, dass wir nun einige dieser interessanten Reaktionen in die Prozessentwicklung oder Entdeckung überführen können."
Das Samarium-Reagenz war bisher auf die Verwendung im Labor beschränkt, da sich bei den Reaktionen eine lästige Samarium-Sauerstoff-Bindung bildet, die die Chemikalie inaktiv macht.
"Bis jetzt war es sehr schwierig, Samarium wieder in seinen aktiven Zustand zu überführen", erklärt die Caltech-Diplomandin Emily Boyd, die im Labor von Jonas Peters, Bren-Professor für Chemie und Direktor des Resnick Sustainability Institute am Caltech, arbeitet. Boyd und Shin sind Co-Autoren der neuen Studie.
"Das Reagenz endet oft mit einer sehr starken Samarium-Sauerstoff-Bindung, die schwer zu brechen ist und das Recycling des Reagenzes erschwert", sagt sie.
Mit anderen Worten: Die Sauerstoffbindung führt die Reaktion in eine Sackgasse. "Es ist, als würde das Samarium-Reagenz faul auf der Couch sitzen und keine Lust auf Arbeit haben", sagt Shin.
"Es fühlt sich in diesem Zustand sehr wohl und möchte in diesem Zustand bleiben", sagt Boyd. "Also haben wir mit verschiedenen Säuren experimentiert, um die Samarium-Sauerstoff-Bindung zu spalten und das Reagenz wieder zum Arbeiten zu bringen."
Frühere Versuche, diese Samarium-Sauerstoff-Bindung zu brechen, erforderten den Einsatz von scharfen Chemikalien. In der neuen Studie gelang es den Forschern, die Bindung mit einer milden Säure zu spalten, die für groß angelegte Reaktionen praktischer ist. Die Säure führt dem gebundenen Sauerstoff ein Proton zu, das ihn in einen Alkohol verwandelt und das Samarium freisetzt.
Boyd sagt, dass sie und ihre Kollegen im Peters-Labor an einer Zusammenarbeit mit dem Reisman-Labor interessiert waren, weil sie in ihren Forschungsstudien zur Stickstofffixierung das Mittel Samariumdiiodid einsetzen. Stickstofffixierung ist der Prozess, bei dem gasförmiger Stickstoff aus unserer Atmosphäre in Verbindungen wie Ammoniak umgewandelt wird, die für Pflanzen (und die Menschen, die diese Pflanzen essen) lebenswichtig sind. Dieser Prozess kann sowohl auf natürliche Weise durch Bakterien als auch künstlich durch chemische Reaktionen erfolgen. Das Peters-Labor entwickelt neue chemische Reaktionen, um Stickstoff künstlich zu fixieren, und zwar auf effizientere und nachhaltigere Weise als bei den derzeit üblichen Verfahren.
"Die Umwandlung von Stickstoff in Ammoniak ist eine Reaktion, an der unser Labor sehr interessiert ist", sagt Boyd. "Wir verwenden das Samarium-Reagenz in unserem Labor, um diese Reaktionen zu untersuchen, aber es wäre unmöglich, dies auf industrielles Niveau zu bringen. In Gesprächen mit der Reisman-Gruppe, die sich auf synthetische organische Chemie spezialisiert hat, beschlossen wir, unsere Kräfte zu bündeln."
Die Zusammenarbeit erwies sich als synergetisch, erklärt Shin: "Ich habe nicht die Fähigkeiten, die Emily hat, und umgekehrt. Diese Kombination ermöglichte es uns, die schwierige Chemie zu verstehen."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.