Im Grenzbereich der chemischen Bindung
Frankfurter Chemiker ist es gelungen, einen Laborexoten zu untersuchen und damit einen Beitrag zum Verständnis der chemischen Bindung zu leisten. Ihre Erkenntnisse zum Elektronentransport in Bor-haltigen organischen Molekülen ist außerdem praxisrelevant.
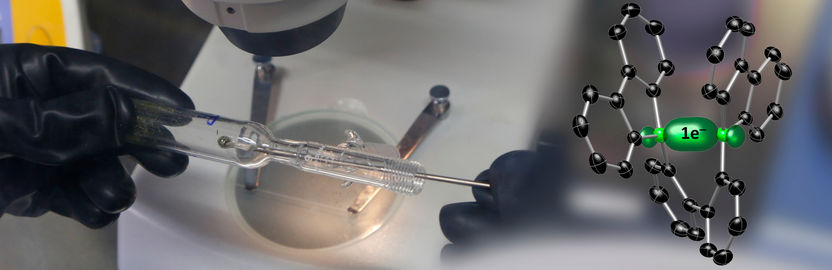
Frankfurter Chemiker konnten ein Bor•Bor-Fragment untersuchen, indem sie es in einen Käfig einsperrten.
Uwe Dettmar
Der Nobelpreisträger Linus Pauling hat schon 1931 darauf hingewiesen, dass zwei Wasserstoffatome zusammengehalten werden können, wenn sie sich lediglich ein Elektron teilen (Einelektron-Zweizentrenbindung). Experimentell sind solche Systeme nur schwer zugänglich. Chemikern der Goethe-Universität ist es nun gelungen, eine Verbindung herzustellen, die eine stabile Bor•Bor Einelektron-Zweizentrenbindung enthält. Die in der Angewandten Chemie publizierten Ergebnisse leisten nicht nur einen Beitrag zum fundamentalen Verständnis der chemischen Bindung, sondern sind auch anwendungsrelevant: Bor-haltige organische Moleküle gelten als Materialien der nächsten Generation für Akkumulatoren, Solarzellen und Organische Leuchtdioden (OLEDs).
„Das Konzept der Elektronenpaarbindung, wie sie im elementaren Wasserstoff, H2, vorliegt, ist jedem Naturwissenschaftler geläufig, während Spezies mit Einelektron-Zweizentrenbindung wie das Wasserstoff-Radikalkation allenfalls als Laborkuriositäten wahrgenommen werden“, so Prof. Matthias Wagner vom Institut für Anorganische und Analytische Chemie der Goethe-Universität. Das liegt daran, dass die Synthese dieser Systeme und ihre Isolierung bei Raumtemperatur äußerst schwierig sind.
Die Frankfurter Arbeitsgruppen von Prof. Matthias Wagner und Prof. Max Holthausen konnten die Schwierigkeiten überwinden, indem sie sich zu Nutze machten, dass man das Bor•Bor-Fragment - im Gegensatz zum Wasserstoff-Radikalkation - in ein größeres Molekül integrieren kann. Dadurch ist es wie in einem Käfig, abgeschirmt. Boratome nehmen bereitwillig Elektronen auf. Positioniert man daher zwei von ihnen in räumlicher Nähe innerhalb einer starren Molekülarchitektur, so lässt sich anschließend ein Elektron gezielt zwischen die beiden Boratome einbetten, wo es von ihnen festgehalten wird.
Erste Hinweise, dass sich eine Bor•Bor Einelektron-Zweizentrenbindung als Folge der Injektion des Elektrons gebildet hatte, ergab die Röntgenstrukturanalyse am Einkristall. Sie zeigte eine signifikante Verkürzung des Bor-Bor-Abstands. Einen entscheidenden Beitrag zur Identifizierung der Einelektron-Zweizentrenbindung lieferte schließlich die quantenchemische Analyse der Elektronendichte, die das einzelne Elektron als fixierendes Bindeglied zwischen den beiden Bor-Atomen zweifelsfrei kennzeichnet.
Von praktischer Bedeutung sind die Untersuchungen vor allem deshalb, weil Bor-haltige organische Moleküle sich derzeit steigenden Interesses in den Materialwissenschaften erfreuen. Will man sie für Akkumulatoren, Solarzellen oder organische Leuchtdioden einsetzen, spielt der Elektronentransport innerhalb dieser Materialien eine wesentliche Rolle. „Dementsprechend stellt sich auch die Frage, unter welchen Umständen Elektronen zwischen Boratomen eingefangen werden und auf diese Weise den Ladungstransport behindern“, erläutert Max Holthausen.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.