Salziger Akku
Natrium-Luft-Akkus mit verbesserter Zyklenfestigkeit dank hochkonzentriertem Elektrolyten
Anzeigen
Ob Smartphone, Laptop oder Elektroauto – ein leistungsfähigerer Akku steht ganz oben auf der Wunschliste der Nutzer. Auf der Suche nach der nächsten Akku-Generation ist der Natrium-Luft-Akku in den Fokus gerückt. Theoretisch sollte er eine bisher unerreichte Leistungsfähigkeit bieten, nur hapert es an der praktischen Umsetzung. Dieser sind Forscher jetzt einen Schritt näher gekommen. Wie sie in der Zeitschrift Angewandte Chemie berichten, könnte eine hochkonzentrierte Elektrolytlösung den Natrium-Luft-Akku stabiler und damit praktikabel machen.
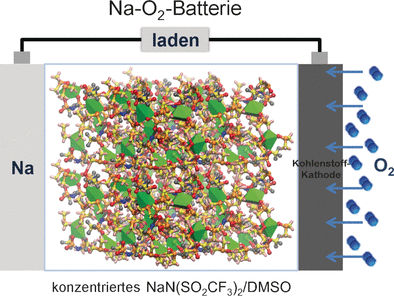
© Wiley-VCH
Auf Alkalimetall-Luft-Akkus werden große Hoffnungen gesetzt, da sie eine besonders hohe theoretische Energiedichte haben. Eine der Elektroden besteht aus dem reinen Alkali-Metall. Beim Entladen gibt sie Elektronen in den Stromkreis und positiv geladene Metall-Ionen an den Elektrolyten ab. Die Gegenelektrode aus porösem Kohlenstoff ist in Kontakt mit der Luft. Hier wird Sauerstoff durch Aufnahme von Elektronen in Gegenwart der Metallionen reduziert. Dabei können verschiedene Metalloxid-Verbindungen entstehen. Bei der Ladung des Akkumulators kehrt sich dieser Vorgang um: An der positiven Elektrode wird Sauerstoff (O2) an die Luft abgegeben, an der negativen Elektrode das Alkalimetall wieder abgeschieden.
Eine Reihe grundsätzlicher Probleme stehen einer praktischen Umsetzung noch im Wege: die unzureichende Wiederaufladbarkeit und zahlreiche Nebenreaktionen, die die Stabilität beeinträchtigen, zudem verstopft bei Ansätzen mit Lithium das entstehende Lithiumperoxid die poröse Elektrode. Das als Rohstoff viel leichter verfügbare Natrium könnte eine bessere Wahl sein: In Natrium/Luft-Zellen entsteht überraschenderweise nicht Natriumperoxid, sondern vor allem Natriumsuperoxid (NaO2), das beim Laden nahezu reversibel wieder in die Elemente zerlegt werden kann.
Notwendig ist ein wasserfreies, aprotisches Lösungsmittel (das keine Wasserstoffionen H+ abspalten kann) für den Elektrolyten. Dimethylsulfoxid (DMSO) wäre für elektrochemische Anwendungen die Wahl – reagiert aber leider allzu gern mit Natrium zu problematischen Reaktionsprodukten.
Mingfu He, Kah Chun Lau, Yiying Wu und ihr Team von der Ohio State University, der California State University sowie dem Argonne National Laboratory (USA) haben dafür jetzt einen Lösungsansatz: Eine sehr hohe Konzentration des organischen Salzes Natriumtrifluormethansulfonimid (NaTFSI) stabilisiert DMSO gegenüber Natrium.
Anhand von Raman-Spektroskopie von NaTFSI/DMSO-Elektrolytlösungen sowie Simulationsrechnungen konnten die Wissenschaftler erklären, warum: In der hochkonzentrierten Lösung entsteht eine Struktur aus locker vernetzten Na(DMSO)3TFSI-Einheiten, die einen großen Anteil der DMSO-Moleküle bindet, sodass nur noch wenige für eine Reaktion zur Verfügung stehen. Das Natrium zersetzt dann vorzugsweise TFSI-Anionen – was vorteilhaft ist, da die Produkte eine passivierende Schutzschicht auf der Natrium-Elektrode bilden.
Die Forscher konstruierten einen kleinen Akku, der gute elektrochemische Eigenschaften zeigte und 150 Lade/Entlade-Zyklen ohne nennenswerte Leistungseinbußen durchlief, während Zellen mit einer verdünnten Elektrolytlösung lediglich 6 Zyklen überstanden.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.

Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.