Neue Regel für die Orbitalbildung bei chemischen Reaktionen entdeckt
Quietschbunt, wolkenförmig oder kugelrund – Elektronenorbitale zeigen, wo und wie sich Elektronen um Atomkerne und Moleküle bewegen. In der modernen Chemie und Physik werden sie für die quantenmechanische Beschreibung und Vorhersage chemischer Reaktionen eingesetzt. Nur wenn sich die Orbitale räumlich und energetisch nahe sind, lassen sie sich kombinieren – dies geschieht, wenn zwei Stoffe miteinander chemisch reagieren. Daneben gibt es aber noch eine weitere Voraussetzung, die erfüllt sein muss, wie Forschende des Forschungszentrums Jülich und der Universität Graz nun herausgefunden haben: Der Ablauf chemischer Reaktionen scheint zusätzlich von der Orbitalverteilung im Impulsraum abhängig zu sein. Die Ergebnisse wurden im Fachmagazin Nature Communications veröffentlicht.
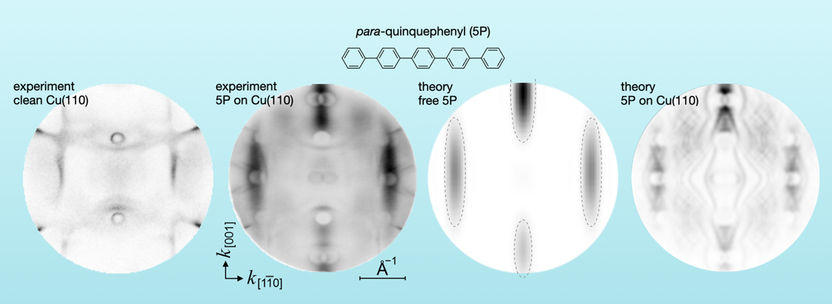
Die experimentelle Impulsverteilung der Photoelektronen von reinem Kupfer und von auf Kupfer adsorbierten para-Chinquephenyl-Molekülen (links) und die theoretische Impulsverteilung von freien Molekülen und von den Molekülen auf Kupfer (rechts).
Forschungszentrum Jülich / X.Yang, S. Soubatch; Graz University / P. Puschnig
Chemische Reaktionen sind letztlich nichts anderes als der Auf- und Abbau von Elektronenbindungen, die üblicherweise mithilfe von Orbitalen beschrieben werden können. Mittels der sogenannten Molekülorbitaltheorie lässt sich so vorhersagen, wie eine chemische Reaktion ablaufen wird. Die Chemiker Kenichi Fukui und Roald Hoffmann erhielten 1981 den Nobelpreis für die starke Vereinfachung des Verfahrens, das seitdem weite Verbreitung und Anwendung gefunden hat.
„Üblicherweise werden die Energie und der Ort der Elektronen analysiert. Mittels der von uns zu diesen Zwecken weiterentwickelten Methode der Photoemissionstomografie haben wir uns aber die Impulsverteilung der Orbitale angeschaut“, erläutert Dr. Serguei Soubatch. Gemeinsam mit seinen Kollegen am Jülicher Peter Grünberg Institut (PGI-3) und der Universität Graz in Österreich hat er in einer Reihe von Experimenten verschiedenartige Moleküle an Metalloberflächen angeheftet und die gemessenen Impulse im sogenannten Impulsraum abgebildet.
„Die Photoemission vieler verschiedener Moleküle auf Metallen, die wir messen, kann auch theoretisch vorhergesagt werden. Modellhaft wird dazu einfach ein freies Molekül verwendet, das nicht mit dem Metall wechselwirkt. Bei der Messung von Oligophenylen auf Kupfer stellten wir jedoch plötzlich fest, dass das experimentelle Ergebnis erheblich von den Vorhersagen abweicht. Bestimmte Teile des Impulsraums blieben unbesetzt“, so Soubatch. Diese Impulsbereiche stimmen mit sogenannten Bandlücken überein, die typischerweise in Edelmetallen auftreten. Und auch einer der beteiligten Stoffe, Kupfer, ist ein solches Edelmetall.
„Im Ergebnis zeigt sich hier ein Auswahlkriterium, das bislang unbekannt war: Orbitale, die sich bei einer chemischen Reaktion zu einem Hybridorbital verbinden, müssen nicht nur hinsichtlich Energie und räumlichen Ausdehnung übereinstimmen, sondern auch eine gleiche Impulsverteilung aufweisen“, erklärt Institutsdirektor Prof. Stefan Tautz.
Für die Arbeit haben die Forschenden Experimente am Elettra-Synchrotron im italienischen Triest durchgeführt. Ein internationales Konsortium unter der Leitung des Forschungszentrums Jülich betreibt dort an einer Beamline ein Photoemissionselektronenmikroskop für orbitaltomografische Messungen.
Die Untersuchungen wurden in Zusammenarbeit mit Prof. Michael. G. Ramsey und dem Theoretiker Prof. Peter Puschnig von der Universität Graz durchgeführt. Letzterer lieferte mit seinen quantenmechanischen Simulationen für das gesamte wechselwirkende System – Moleküle und Metalloberfläche – den Schlüssel zur Erklärung des neu gefundenen Auswahlkriteriums.
Originalveröffentlichung
Meistgelesene News
Originalveröffentlichung
Momentum-selective orbital hybridisation; Xiaosheng Yang, Matteo Jugovac, Giovanni Zamborlini, Vitaliy Feyer, Georg Koller, Peter Puschnig, Serguei Soubatch, Michael G. Ramsey, F. Stefan Tautz; Nature Communications (2 September 2022)
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.