Die kleinsten Eiskristalle der Welt
Ein raffiniertes Experiment deckt auf, ab wie vielen Molekülen Wasser eine kristalline Ordnung bildet
Auch Eiskristalle fangen mal klein an, und sogar kleiner als bisher gedacht. Schon 475 Wassermoleküle bilden eine echte kristalline Ordnung, erste Ansätze davon sind bereits ab 275 Molekülen zu erkennen, wie eine Kooperation aus Göttinger und Prager Wissenschaftlern herausgefunden hat. Zuvor galten etwa 1000 Moleküle als Minimum für einen vollständigen Kristall. Die neue Untergrenze für Eisklümpchen haben die Forscher um Thomas Zeuch von der Universität Göttingen mit einem Experiment bestimmt, das Udo Buck vom Göttinger Max-Planck-Institut für Dynamik und Selbstorganisation entwickelt hat.

Am Ursprung des perfekten Kristalls: Wasser kristallisiert in einer sechszähligen Symmetrie, die an jeder Schneeflocke zu erkennen ist. Diese Ordnung bildet sich bereits in Wasserclustern mit 475 Molekülen aus, die mit einer Schneeflocke noch keine Ähnlichkeit haben.
© Science Photo Library
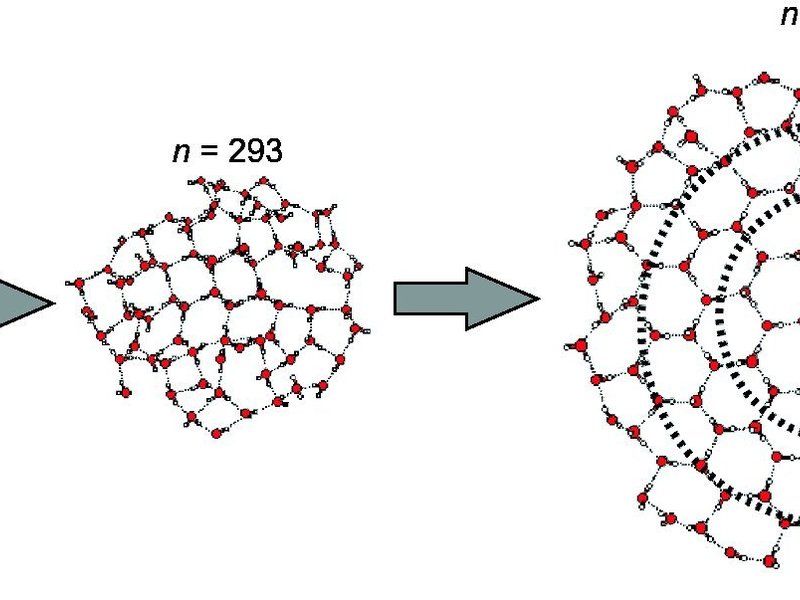
Mit wachsender Größe finden sehr kalte Cluster ausWassermolekülen zur Ordnung eines echten Eiskristalls. Bei 123 Wassermolekülen (links) sind Cluster noch völlig ungeordnet – wie eine erstarrte Flüssigkeit. Bei knapp 300 Molekülen (Mitte) ist im Kern des Clusters schon die sechseckige Ordnung des Eiskristalls erkennbar. Bei 600 Molekülen (rechts) ist der Eiskristall im Inneren perfekt ausgebildet, nur die äußere Schicht ist noch ungeordnet (amorph).
© Udo Buck

Nichts ist für uns so selbstverständlich wie das Verhalten von Wasser. Dazu gehört die sommerliche Erfahrung, dass eine im Gefrierfach vergessene Wasserflasche platzt. „Dabei ist das ganz eigenartig“, kann Udo Buck sich nach seiner langen Wissenschaftlerkarriere noch begeistern: „Wasser ist witzigerweise einer der wenigen uns bekannten Stoffe, der im festen Zustand ein größeres Volumen als im flüssigen Zustand einnimmt.“ Mit dem kleinsten Wassereiskristall hat der Forschungsgruppenleiter am Max-Planck-Institut für Dynamik und Selbstorganisation in Göttingen ein wegweisendes Ergebnis erzielt. Seine Mitautoren, darunter die Gruppe von Thomas Zeuch am Institut für Physikalische Chemie der Universität Göttingen, und ein Forscher von der Technischen Universität Prag, haben dazu ein von Buck seit den 2000er-Jahren entwickeltes Experiment weiter verfeinert.
Nun hat das Team ein bislang ungelöstes wissenschaftliches Rätsel geknackt, nämlich die Frage, wie viele Wassermoleküle mindestens zusammenkommen müssen, damit sie einen echten Eiskristall formen können. „Bei 275 Wassermolekülen geht es los“, lautet die verblüffend präzise Antwort von Buck, „und bei 475 Molekülen ist der Kristall vollständig fertig.“ Das sei durchaus unerwartet, schiebt Buck nach, denn bislang habe die Wissenschaft eine minimale Clustergröße von etwa 1000 Wassermolekülen vorausgesetzt. Unter Clustern verstehen Physiker und Physikochemiker Konglomerate aus wenigen, noch abzählbaren Molekülen. Die Eigenschaften dieser Nanogebilde liegen zwischen denjenigen einzelner Moleküle und der Welt großer Festkörper zum Anfassen, die aus vielen Milliarden Molekülen bestehen. Ein besseres Verständnis des Kristallisationsprozesses hilft Klimaforschern
Allerdings untersuchte die Göttinger Kooperation nicht das Entstehen von Eis aus flüssigem Wasser. Ihre Entdeckung gibt Einblicke in die Vorgänge, bei denen Wasserdampf bei tiefen Temperaturen direkt zu winzigen Eiskristallen kondensiert. „Solche Prozesse spielen in den oberen Atmosphärenschichten eine wichtige Rolle“, betont Buck: „aber auch in unserem Planetensystem.“ Das neue Ergebnis könnte also der Klimaforschung helfen, ihre Modelle der Atmosphäre zu verbessern. Aber was fanden die Forscher nun genau heraus?
In Eiskristallen sortieren sich die Wassermoleküle zu einem sechseckigen, wissenschaftlich präziser gesagt, hexagonalen Raumgitter. Dabei baut jedes Wassermolekül chemische Bindungen, sogenannte Wasserstoffbrücken, zu jeweils vier Nachbarmolekülen auf. Dieses wabenförmige Kristallgitter von Wassereis benötigt mehr Raum als das flüssige Wasser, was außergewöhnlich ist. Solange die Wassercluster noch nicht die Mindestgröße für einen Kristall erreicht haben, bringt das Göttinger Experiment sie in ein Dilemma. Die Versuche finden bei ungefähr minus 180 bis minus 150 Grad Celsius statt – für eine Flüssigkeit sind die Moleküle also viel zu kalt. Für einen Kristall sind sie aber noch zu wenige. Aus der Zwickmühle kommen die kleinen Cluster, indem sie eine Art in der Kälte gestockte Flüssigkeit bilden: Sie bilden ein eher unordentliches, „amorphes“ Raumgitter.
Wächst der Cluster nun, können die Wassermoleküle in seinem Kern irgendwann vom ungeordneten chemischen Spiel in die kristalline Ordnung wechseln, in der sie alle jeweils vier Nachbarn an die chemische Hand nehmen. So entstehen bei 275 Wassermolekülen im Inneren des Clusters erste Ansätze eines echten Eiskristalls mit sechseckiger Struktur. Anfangs ist diese Struktur noch etwas deformiert. Doch mit wachsender Clustergröße wächst dieses Innenleben zu einem schön geordneten Eiskristall, während die Außenschichten noch amorph bleiben. „Bei 475 Molekülen ist es ganz innen schon perfekt“, sagt Buck.
Dieser Einblick in das Entstehen von Eiskristallen war nur mit einem ausgefeilten Experiment möglich. Normalerweise durchleuchten Wissenschaftler Kristalle mit Röntgenstrahlen: Diese werden von den Gittern gebeugt. Dabei entstehen charakteristische Muster der Strahlung, die Informationen über den Aufbau der Gitter liefern. In den Schwingungen der Moleküle offenbart sich die Kristallstruktur
Doch diese Signale seien zu schwach für die genaue Untersuchung der kleinen Wassercluster, erklärt Thomas Zeuch. Dagegen liefere die Schwingung zwischen dem Sauerstoffatom und dem Wasserstoffatom eines Moleküls ein viel kräftigeres Signal. Die Frequenz dieser Molekülschwingung liegt im Infraroten, also bei langwelligem Licht, und die Wirkung dieser Strahlung misst die Apparatur. Entscheidend ist dabei, dass sich das Infrarotsignal durch die Wasserstoffbrückenbindung zwischen dem Wasserstoffatom des einen und dem Sauerstoffatom eines anderen Moleküls deutlich verschiebt, sobald sich das sechseckige Kristallgitter bildet. Das ist der Fingerabdruck des echten Wassereises, den die Göttinger Wissenschaftler nun erstmals an Clustern aus einigen hundert Wassermolekülen nachweisen konnten.
Diese Infrarotspektroskopie solcher kleiner Cluster funktioniert allerdings nur mit einigen Tricks. Zuerst erzeugt das Experiment einzelne, kalte Cluster. Diese Cluster fliegen dann mit mehr als Schallgeschwindigkeit durch eine Kammer, in der sie jeweils ein einzelnes Natriumatom aufsammeln. Anschließend fliegen sie etwa 240 Mikrosekunden (Millionstel Sekunden) lang weiter bis zur eigentlichen Messung. Das angedockte Natriumatom sei dabei ganz entscheidend, erläutert Thomas Zeuch. Es erlaubt nämlich, die Cluster in der gewünschten Größe, zum Beispiel eben aus 275 Wassermolekülen, sanft zu ionisieren, mit einem elektrischen Feld zu sortieren und gezielt zu messen. Die nächsten Versuche sollen klären, wie andere Stoffe kristallisieren
Das Natriumatom am Wassercluster hat zudem eine zweite, ziemlich komplexe Funktion. „Es ist eine Art Fotopapier“, sagt Zeuch, um seine Rolle zu veranschaulichen. „Wir bestrahlen die Cluster mit dem Natriumatom zuerst mit dem Infrarotlicht“, sagt der Physikochemiker: „Dann ,entwickeln‘ wir es mit einem Laserpuls aus ultraviolettem Licht.“ Allerdings gibt das Natriumatom bei dieser Kombination von Laserlicht verschiedener Frequenz natürlich kein räumliches Foto: Stattdessen liefert es ein Infrarotspektrum des winzigen Wasserclusters. Dieser entscheidende Trick war der Durchbruch.
Das Grundprinzip des Experiments hatte Udo Buck am Max-Planck-Institut für Dynamik und Selbstorganisation entwickelt. Heute steht die Apparatur bei Thomas Zeuch an der Uni Göttingen. Die Wissenschaftler dieser Gruppe haben sie zusammen mit theoretischer Unterstützung aus Prag so weiter entwickelt, dass die Erforschung von Clustern aus einigen hundert Wassermolekülen erst möglich wurde. Die Forscher wollen mit Experimenten nun auch die Kristallisation anderer Stoffe und deren Oberflächeneigenschaften – wo möglich – auf´s Molekül genau untersuchen. Zeuch ist von dem neuen Experimentierverfahren aber auch deshalb so begeistert, weil es sich nicht nur auf Wassercluster anwenden lässt. Es eröffnet ein völlig neues Experimentierfeld.
Originalveröffentlichung
Cristoph C. Pradzynski, Richard M. Forck, Thomas Zeuch, Petr Slavíček, Udo Buck: A fully size-resolved perspective on the crystallization of water clusters Science, 21. September 2012
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!