Wenn Moleküle miteinander tanzen
Einfache Reaktion zur Herstellung von Pyridinen
Der Chemiker Nuno Maulide von der Universität Wien beschreitet neue Wege bei der Herstellung von Pyridinen, wichtigen Synthesebausteinen für die Arzneimittelforschung. Er hat eine Variante der sogenannten Cycloadditionen entwickelt, die gänzlich ohne Katalysatoren auskommt – ein Durchbruch in der Pyridinsynthese. Dabei selektiert er die einzelnen Bausteine ähnlich einer Choreographie eines Tanzes so, dass die chemischen "Tanzpartner" nur nacheinander und zu einem bestimmten Zeitpunkt zur Synthese beitragen und damit auch das richtige "Produkt" ergeben.
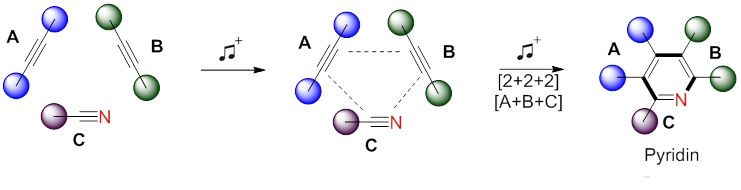
Eine Cycloaddition ist wie ein Tanz.
Copyright: Universität Wien

Dem Team um Nuno Maulide von der Universität Wien ist es gelungen, eine wesentlich einfachere Reaktion zur Herstellung von Pyridinen zu finden.
Copyright: Universität Wien

Benzen (veraltet: Benzol) besteht aus sechs kreisförmig angeordneten Kohlenstoffatomen und ebenso vielen Wasserstoffatomen. Es ist eine organische Verbindung, die ChemikerInnen seit fast zwei Jahrhunderten fasziniert: Wird nämlich einer dieser Kohlenstoffe durch ein Stickstoffatom ersetzt, entsteht Pyridin – ein bedeutender Synthesebaustein für die Arzneimittel- und Herbizidherstellung. Pyridin wurde erstmals im Jahr 1851 aus Knochenöl isoliert und gilt seither sowohl als wertvolles und vielseitiges Endprodukt als auch als ein gängiges Lösungsmittel für chemische Reaktionen.
Viele der meinstverkauften Pharmazeutika enthalten das Strukturmotiv der Pyridine. "Es ist vermutlich das häufigste Motiv, das man in zugelassenen Arzneien finden kann", erklärt Nuno Maulide: "Demnach ist es nicht überraschend, dass in den letzten Jahrzehnten viele ChemikerInnen an neuen Strategien für die Darstellung von Pyridinen geforscht haben", so der portugiesische Chemiker.
Eine Cycloaddition ist wie ein Tanz
Der flexibelste Weg, Pyridine mit vielen verschiedenen Substituenten herzustellen, ist die sogenannte [2+2+2] Cycloaddition. Bei dieser Reaktion kommen drei verschiedene Reaktanden zusammen, die jeweils zwei Atome beisteuern, und dadurch in einem einzigen Schritt einen Ring aus sechs zusammenhängenden Atomen aufbauen. "Man kann es mit einem Tanz vergleichen: Drei Menschen treffen sich, reichen sich die Hände und bilden so einen Ring", erklärt Maulide.
Der chemische Tanz braucht Selektivität
Das Hauptproblem dieses einfachen Grundkonzepts ist die Selektivität. "Zwei Bedingungen müssen erfüllt werden, wenn dieser 'Tanz' für ChemikerInnen nützlich sein soll. Erstens müssen sich die drei richtigen Menschen finden und zweitens müssen sich diese Menschen auch in der richtigen Reihenfolge und Ausrichtung anordnen", erklärt Saad Shaaban, Co-Autor der Studie und Doktorand am Institut für Organische Chemie der Universität Wien. "Nur die richtige Choreographie liefert das richtige Produkt", ergänzt Maulide. Bislang konnte diese Selektivität nur unter bestimmten Voraussetzungen und nur mithilfe eines Metallkatalysators erreicht werden. "Unsere neue, hochselektive [2+2+2] Cycloaddition schafft es, gänzlich ohne solche Katalysatoren auszukommen – ein Durchbruch in der Pyridinsynthese", freut sich Maulide.
"Das Prinzip hinter unserem erfolgreichen Design ist denkbar einfach", erläutert der Portugiese: "Wir stellen die einzelnen reaktiven Spezies hintereinander her – somit kann zu jedem gegebenen Zeitpunkt nur der von uns gewünschte Reaktionspartner zum Kreis hinzustoßen". Um bei der Tanzanalogie zu bleiben: Die erste Person sucht seinen ersten Partner sorgfältig aus der großen Menge, anstatt blind zu wählen. Die neu gebildete Zweiergruppe stellt in der Folge noch höhere Ansprüche bei der Wahl des dritten Partners und selektiert genau. "Selektivität ist nichts weiter als die Kunst, wählerisch zu sein!", lacht Maulide.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.

Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.






























































