Forscher finden molekularen Schutzmechanismus gegen lichtinduzierte Schädigungen
Ein internationales Team aus Forschenden des Helmholtz-Zentrum Berlin (HZB) sowie aus Schweden und den USA hat einen Mechanismus untersucht, der Biomoleküle wie die Erbsubstanz DNA gegen Schädigung durch Licht schützt. Sie beobachteten, wie die Energie der einfallenden Photonen im Molekül aufgenommen wird ohne wichtige Bindungen des Biomoleküls zu beschädigen. Die Experimente fanden am Freie Elektronen-Laser LCLS in Kalifornien und an der Synchrotronquelle BESSY II des HZB in Berlin statt, wo mit der Methode der resonanten inelastischen Röntgenstreuung, RIXS, ein sehr empfindliches Messverfahren bereit steht.
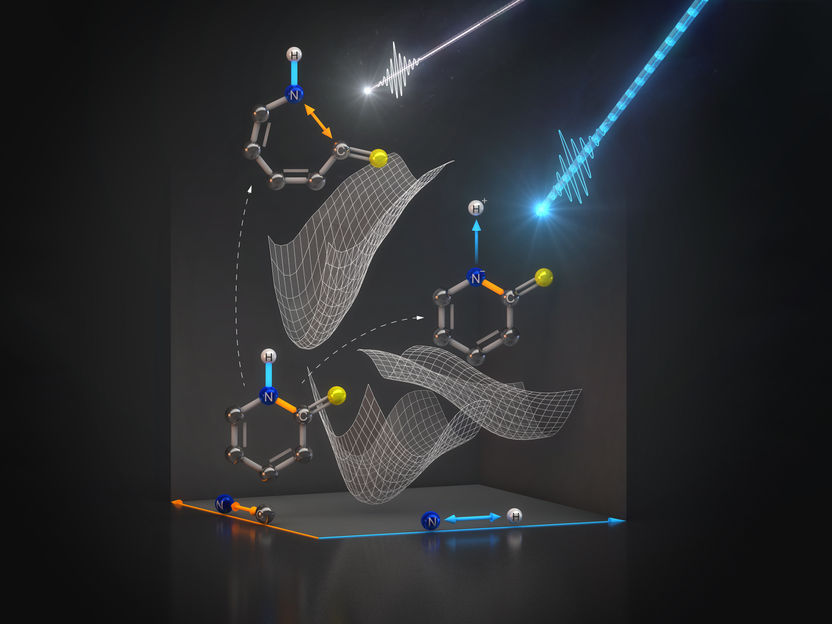
Die Experimente zeigen: Lichtpulse können Wasserstoffkerne ablösen, ohne weitere Bindungen im Molekül zu zerstören.
Th. Splettstösser/HZB
Biomoleküle wie die Erbsubstanz DNA benötigen Schutzmechanismen gegen energiereiches Licht. Denn UV-Anteile aus dem Sonnenlicht würden sonst rasch dazu führen, dass Bindungen brechen und Moleküle zerfallen. Der so genannte Protonentransfer spielt dabei eine wichtige Rolle. Mit ihm kann ein DNA-Molekül die über das Licht eingestrahlte Energie wieder abgeben – dabei löst sich ein einzelnes Proton (Wasserstoffkern) – und andere chemische Bindungen bleiben erhalten.
Um den Prozess im Detail zu untersuchen, hat eine internationale Kooperation um Prof. Dr. Alexander Föhlisch, Institutsleiter am Helmholtz-Zentrum Berlin, in Kalifornien am LCLS-Laser des SLAC National Accelerator Laboratory und an der Berliner Synchrotronquelle BESSY II des HZB Experimente durchgeführt: Sie untersuchten ein verhältnismäßig einfaches Molekül, das 2-Thiopyridon (2-TP). Dieses Molekül hat ähnliche Eigenschaften wie die Bausteine der DNA und dient in der Bioforschung deshalb als Modellmolekül.
Die Forschergruppe regte zunächst gezielt das Stickstoff-Atom im Molekül mit sehr kurzen Röntgenpulsen im Femtosekundenbereich (10 -15 s) an. Die Ergebnisse, die nun im Fachblatt Angewandte Chemie publiziert sind, zeigen im Detail, wie sich nach der Anregung mit dem Lichtpuls das an das Stickstoff-Atom gebundene Proton ablöst.
"Erst einmal wollten wir diese Prozesse an einem einfachen Modellsystem untersuchen,” sagt Erstautor Sebastian Eckert, der bei Alexander Föhlisch an der Universität Potsdam und am Helmholtz-Zentrum Berlin seine Doktorarbeit schreibt. " Das Modellsystem 2-Thiopyridon ist geeignet, weil das Molekül klein genug ist, um es zu verstehen und nur ein einziges Stickstoff-Atom besitzt. Nur durch den Vergleich zwischen den FEL-Messungen und Experimenten am Synchrotron BESSY II ließ sich der Mechanismus eindeutig zuordnen." Dabei hatte das Team erstmals auch die Methode der so genannten inelastischen Röntgenstreuung, RIXS, an BESSY II angewandt, um molekulare Veränderungen um das Stickstoff-Atom herum zu beobachten, die mit dem raschen Protonentransfer zusammenhängen und extrem schnell, innerhalb von Femtosekunden, ablaufen.
Durch die Kombination der Experimente mit theoretischen Simulationen konnte letzlich der Reaktionspfad herausgearbeitet werden. Diese Berechnungen führte der Doktorand Jesper Norell und Prof. Dr. Michael Odelius der Universität Stockholm im Rahmen des Helmholtz Virtuellen Instituts „Dynamic Pathways in Multidimensional Landscapes“ durch.
Originalveröffentlichung
"Ultrafast Independent N-H and N-C Bond Deformation Investigated with Resonant Inelastic X-ray Scattering" Sebastian Eckert;, Jesper Norell;, Piter S. Miedema, Martin Beye,Mattis Fondell, Wilson Quevedo, Brian Kennedy, Markus Hantschmann,Annette Pietzsch, Benjamin Van Kuiken, Matthew Ross,Michael P. Minitti, Stefan P. Moeller, William F. Schlotter, Munira Khalil, Michael Odelius, Alexander Föhlisch; Angewandte Chemie, International Edition; 2017
Meistgelesene News
Originalveröffentlichung
"Ultrafast Independent N-H and N-C Bond Deformation Investigated with Resonant Inelastic X-ray Scattering" Sebastian Eckert;, Jesper Norell;, Piter S. Miedema, Martin Beye,Mattis Fondell, Wilson Quevedo, Brian Kennedy, Markus Hantschmann,Annette Pietzsch, Benjamin Van Kuiken, Matthew Ross,Michael P. Minitti, Stefan P. Moeller, William F. Schlotter, Munira Khalil, Michael Odelius, Alexander Föhlisch; Angewandte Chemie, International Edition; 2017
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.





























































