Nanodiamanten als Energiematerialien: kleine „Anhänger“ mit großer Wirkung
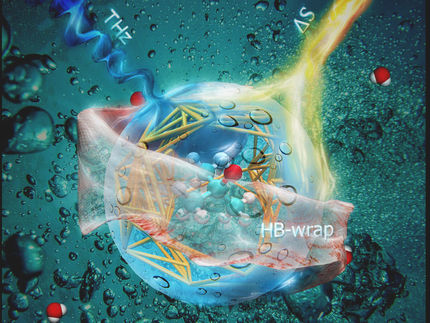
Ein internationales Forscherteam hat neue Einblicke in die Wechselwirkungen zwischen Nanodiamanten und Wassermolekülen gewonnen. Durch Versuche an Synchrotronquellen konnten sie feststellen, dass kleine Molekülgruppen auf den Nanodiamantoberflächen großen Einfluss auf das Wasserstoffbrücken-Netzwerk ausüben. Dies könnte insbesondere für (photo)-katalytische Anwendungen interessant sein, zum Beispiel für die Produktion von solaren Brennstoffen mit Kohlendioxid und Licht.
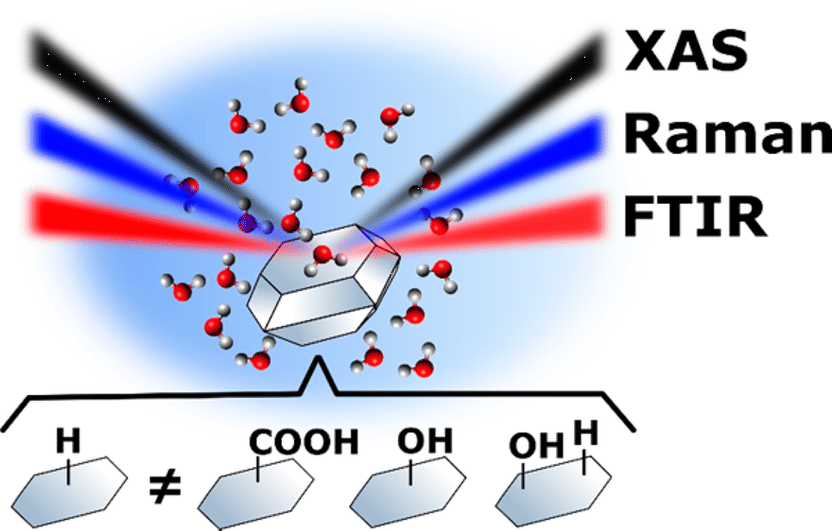
ie Nanodiamanten in Lösung wurden mit unterschiedlichen Molekülgruppen modifiziert.
HZB
Diamanten kennen wir als durchsichtige schimmernde Kristalle, die in Wasser rasch versinken. Aber tatsächlich kommt es darauf an, wie groß die Diamantkristalle sind. Die allerkleinesten solcher Kristalle, die nur wenige Nanometer dick sind, schweben in Wasser und bilden eine ölige, schwarze Mischung, ein so genanntes Kolloid. Solche Nanodiamanten in Lösung lassen sich vielseitig anwenden, zum Beispiel in der medizinischen Forschung oder als metall-freie Katalysatoren für die Umwandlung von Licht in chemische Energie.
Was passiert zwischen Nanodiamanten und Wasser?
Dabei spielen die Wechselwirkungen zwischen den Nanopartikeln und den umgebenden Wassermolekülen eine extrem wichtige Rolle. Sie entscheiden darüber, ob das Kolloid stabil bleibt oder sich entmischt, bestimmen die optischen Eigenschaften, aber vor allem auch die chemische und katalytische Reaktivität. Was jedoch im Detail an den Grenzflächen zwischen Nanodiamanten und Wassermolekülen passiert, war bislang kaum bekannt.
Oberflächen mit Molekülen modifiziert
Nun hat eine internationale Kooperation zwischen russischen, japanischen, amerikanischen, französischen und deutschen Forschungsgruppen erstmals die Wechselwirkungen zwischen Nanodiamanten und Wassermolekülen genauer untersucht. Durch die Kombination verschiedener spektroskopischer Methoden an den Synchrotronquellen BESSY II am HZB in Berlin und an UVSOR III in Japan gelang es ihnen, die Wechselwirkungen im Einzelnen aufzuschlüsseln. Dafür modifizierten sie die Oberflächen der Nanodiamanten, mit Wasserstoff (-H) oder kleinen Molekülen, die an den Oberflächen der Nanodiamanten andockten, zum Beispiel Karboxyl-Gruppen (-COOH) und Hydroxylgruppen (–OH).
H-Atome könnten katalytische Aktivität steigern
Dabei zeigte sich, dass die Oberflächen-Gruppen einen unterschiedlich starken Einfluss auf die Wasserstoffbrücken-Netzwerke im Kolloid ausüben. Während Hydroxyl- und Karboxyl-Gruppen an den Nanodiamanten die Anordnung der umgebenden Wassermoleküle nur wenig veränderten, führten angehängte Wasserstoffatome zu einer deutlichen Veränderung: „Die Wasserstoffbrücken zwischen den Wassermolekülen sind viel schwächer als die, die man in normalem Wasser findet“, sagt der HZB-Physiker Dr. Tristan Petit. Dies könnte mit der Anreicherung von Elektronen an den Grenzflächen zwischen Nanodiamanten und Wasser zusammenhängen, vermuten die Forscher. „Diamant-Oberflächen mit angelagerten Wasserstoffatomen setzen effizient Elektronen in Wasser frei, was die Reduktion von CO2 in Wasser mit Hilfe von UV-Licht ermöglichen könnte“, erklärt Petit. „Die einzigartige Struktur von Wasser, die mit den hydrogenierten Oberflächen einhergeht, spielt sicher eine bislang unterschätzte Rolle in diesem aufregenden Prozess.”
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!