"Molekularer Scharfmacher" entschlüsselt
Kristallstruktur vom Aktivator-Protein Furin aufgklärt
Die dreidimensionale Struktur von Furin, einem Protein, das für die Aktivierung zahlreicher wichtiger Eiweißstoffe in lebenden Zellen zuständig ist, haben Wissenschaftlern des Max-Planck-Instituts für Biochemie in Martinsried gemeinsam mit amerikanischen und britischen Forschern aufgeklärt (vgl. Nature Structural Biology, Juli 2003). Furin spielt bei so unterschiedlichen Erkrankungen und Infektionen, wie Ebola, AIDS oder Anthrax, eine wichtige Rolle. Deshalb stellt Furin nicht erst seit dem Einsatz von Anthrax-Erregern als Biowaffe ein sehr interessantes Zielmolekül für Medikamente dar. Heute gibt es bereits eine Reihe von Hemmstoffen, mit denen sich die Aktivierung von Proteinen durch Furin unterdrücken lässt. Doch um diese Hemmstoffe zu wirksamen Medikamenten zu entwickeln, ist die Kenntnis der genauen räumlichen Struktur von Furin von großer Bedeutung. Wenn Bakterien oder Viren andere Organismen befallen, sind sie bei dieser Infektion häufig auf die Ressourcen in den Zellen ihres Wirts angewiesen, damit sie sich dort vermehren können. Bei einer Reihe von gefährlichen Krankheiten wie Ebola, AIDS, Anthrax und Diphtherie benutzen die Krankheitserreger das Protein Furin aus den Säugetierzellen, um ihre Strategien mit fatalen Folgen für den Infizierten in Gang zu setzen.
Furin kommt überall in unserem Körper vor und sorgt dafür, dass zahlreiche andere Proteine ihre natürlichen Funktionen ausüben können. Dieses Protein tritt sowohl auf der Oberfläche von Zellen als auch in ihrem Innern auf und überführt andere Proteine, die als inaktive Vorstufen in den Zellen vorliegen, in ihre biologisch aktive Form. Hierzu spaltet es entweder diese Vorstufen oder verkürzt sie an einem Ende, indem es die Aminosäurenkette des Proteins an einer ganz bestimmten Stelle durchtrennt (Proteolyse). Auch Furin selbst entsteht zuerst als inaktive Vorstufe, kann sich dann allerdings selbst proteolytisch spalten und braucht somit keine weiteren Proteine für seine Aktivierung. Proteine, die andere Proteine durch Spaltung oder Verkürzung aktivieren, zählen zur Familie der Proteinasen. Innerhalb der Proteinasen gehört Furin zu einer speziellen, Kalzium-abhängigen Unterfamilie, den so genannten Proprotein-Konvertasen.
Zu den Zielproteinen (Substraten) von Furin gehören Vorstufen von ganz unterschiedlichen Proteinen, wie zum Beispiel Wachstumsfaktoren, Hormone, Rezeptoren und Plasmaproteine, die zumeist an sehr wichtigen Aufgaben wie der embryonalen Entwicklung oder der Regulation verschiedener Körperfunktionen (Homöostase) beteiligt sind. Doch dieser Art der biologischen Aktivierung bedienen sich in einer Zelle nicht nur körpereigene Proteine, sondern auch Bakterien und Viren. Bei einer Infektion benutzen diese das Furin ihres Wirts dazu, um ihre Proteinvorstufen in aktive Proteine umzuwandeln: Erst dadurch wird beispielsweise bei Anthrax und Diphtherie die Aktivierung und Aufnahme der Erregergifte in die Zelle möglich. Doch Furin kann auch an einer fehlerhaften Aktivierung körpereigener Proteine beteiligt sein, was dann zur Entstehung von Krebs oder der Alzheimerschen-Krankheit führt.
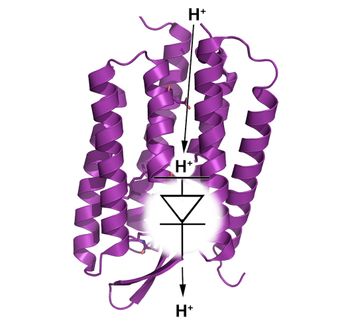
Stefan Henrich hat es nun mit seinen Kollegen aus der Abteilung Strukturforschung am Max-Planck-Institut für Biochemie, Martinsried, geschafft, das Furin-Protein aus der Maus zu kristallisieren und seine dreidimensionale Struktur mit Hilfe der Röntgengenstrukturaufklärung zu bestimmen. Damit gelang den Forschern zugleich die erstmalige Kristallisation eines Mitglieds der Proprotein-Convertase-Familie. Das Protein wurde in enger Zusammenarbeit mit einer Wissenschaftlergruppe um Iris Lindberg am Health Sciences Center der Louisiana State University in New Orleans (Louisiana, USA) gewonnen. Die dreidimensionale Struktur ermöglicht den Forschern tiefe Einblicke in die verschiedenen Bereichen des Proteins. So besteht Furin aus einer für die Spaltung seiner Zielproteine wichtigen Region (katalytische Domäne), die durch einen weiteren Bereich, die so genannte P?Domäne, stabilisiert wird. Beide Regionen sind für die richtige Funktion, also das Spalten von Zielproteinen, unerlässlich. Von großem Interesse ist aber insbesondere das aktive Zentrums, jener Teil der katalytischen Region, an die Zielproteine binden und wo die proteolytische Spaltung tatsächlich erfolgt. Hier liefern die jetzt gewonnenen Strukturdaten wichtige Anhaltspunkte, welche hohen Ansprüche Furin an die Erkennung der Spaltregion in seinen Zielproteinen stellt: Nur wenn diese Substratmoleküle eine ganz bestimmte Form aufweisen, passen sie in das aktive Zentrum, wie ein Schlüssel in das Schloss. Während andere Proteinasen oftmals viele verschiedene Formen von Substraten zulassen, müssen bei Furin vor der beabsichtigten Spaltstelle positiv geladene Bausteine (basische Aminosäuren) einer bestimmten Größe vorhanden sein. Diese basischen Aminosäuren reichen dann tief in das negativ geladene aktive Zentrum des Proteins und es kommt zur Spaltung des Zielmoleküls. Das so geschnittene Molekül zerfällt in zwei Teile, löst sich wieder vom aktiven Zentrum und gibt dieses für das nächste Zielmolekül frei.
Genau an dieser Stelle ist die dreidimensionale Struktur besonders interessant für die medizinische Forschung und die Entwicklung von neuen Medikamenten. Gelingt es nämlich Hemmstoffe zu finden, die genau in das aktive Zentrum von Furin passen und dieses blockieren, könnte man die proteolytische Spaltung der Zielmoleküle verhindern. Hierzu bindet ein solcher Hemmstoff an das Furin, kann dort aber nicht umgesetzt werden und verhindert daher dauerhaft die Umsetzung weiterer Zielmoleküle. Bereits jetzt kennt man natürliche und synthetische Hemmstoffe, mit denen sich das Absterben von Zellen verhindern lässt, das durch bakterielle Gifte, wie das Anthrax-Toxin, verursacht wird. Mit der genauen räumlichen Struktur des Furins kann man nun die Bindung der Hemmstoffe im Computermodell simulieren und die Hemmstoffe exakt auf die Form des aktiven Zentrums zuschneiden. Je besser ein Hemmstoff in das aktive Zentrum passt, umso besser kann dieser die natürlichen Zielmoleküle nachahmen, sie verdrängen und die Aktivität von Furin herabsetzen. Eine Blockade von Furin durch genau angepasste Hemmstoffe würde bei einer Infektion die Reifung der bakteriellen oder viralen Proteine verhindern und so den tödlichen Verlauf einer Infektion verhindern, den Verlauf einer Krankheit abschwächen bzw. ihre Heilung beschleunigen.
Mit der exakten Bestimmung der Struktur von Furin, einer der wichtigsten Proteinasen, die für die Aktivierung vieler verschiedener Proteine verantwortlich ist, haben die Martinsrieder Wissenschaftler den Ausgangspunkt für die Entwicklung neuer Medikamentente gegen Krankheiten wie Krebs, Alzheimer und Anthrax geschaffen. Die am Beispiel der Maus gewonnenen Erkenntnisse lassen sich sehr gut auf das menschliche Furin übertragen, da beide Proteine fast identisch sind. Mehr noch, Furin ist der bekannteste Vertreter der Familie der Proprotein-Convertasen, so dass sich die aus der räumlichen Struktur gewonnenen Ergebnisse mit großer Wahrscheinlichkeit auch auf seine anderen Familienmitglieder verallgemeinern lassen. Im Gegensatz zu dem im gesamten Körper vorkommenden Furin ist der Wirkkreis dieser Furine häufig auf bestimmte Gewebe oder Organe, wie beispielsweise das Gehirn, beschränkt. Entsprechend lassen sich dafür spezifische Medikamente entwickeln, die nur lokal im Vorkommensbereich einer bestimmten Furin-Verwandten wirken.
Originalveröffentlichung:
Stefan Henrich, Angus Cameron, Gleb P. Bourenkov, Reiner Kiefersauer, Robert Huber, Iris Lindberg, Wolfram Bode und Manuel E. Than The crystal structure of the proprotein processing proteinase furin explains its stringent specificity Nature Structural Biology, 10(7): 520-526, July 2003