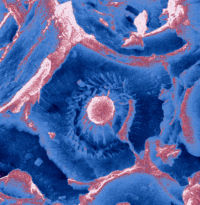
Harte Schale, weicher Kern
Enzym als Nanoreaktor für die Halbleitersynthese bei Raumtemperatur
Halbleiter sind aus unserer modernen Technik nicht mehr wegzudenken. Oxidische Halbleiter, wie etwa Zinkoxid (ZnO), sind beispielsweise Materialien der Wahl als durchsichtige leitende Schichten für blaue Leuchtdioden, Flüssigkristallbildschirmen oder Solarzellen. Die großtechnische Herstellung solcher oxidischer Halbleiter ist ein energieintensiver Prozess. Um den Energieverbrauch zu senken, ist man auf der Suche nach Herstellprozessen, die bei milden Bedingungen laufen. Forscher vom Hunter College der City University of New York haben nun einen neuen Ansatz entwickelt, der Zinkoxid bei Raumtemperatur liefert. Wie Hiroshi Matsui und Roberto de la Rica in der Zeitschrift Angewandte Chemie berichten, nutzen sie das Enzym Urease als "Nanoreaktor" zur Herstellung kristalliner Zinkoxid-Nanoschalen.
Die Urease kommt beispielsweise in Pflanzensamen, Bakterien und verschiedenen Meerestieren vor. Sie spaltet Harnstoff in Kohlendioxid und Ammoniak. Ammoniak ist ein basischer Stoff. Ist die Urease aktiv, steigt der pH-Wert auf der Oberfläche des Enzyms an.
Die Urease hat, aufgrund ihrer negativen Ladungen auf der Oberfläche, eine hohe Affinität zu positiv geladenen Metallionen. In einer Zinknitrat-Lösung reichern sich die Zinkionen um die Urease herum an. Der lokale pH-Wert auf der Enzymoberfläche lässt sich fein auf Werte einjustieren, die für die Bildung von Zinoxid ideal sind. Der Mechanismus des Aufkonzentrierens der Zinkionen bei passendem pH-Wert katalysiert die Entstehung und das Wachstum von ZnO-Kristallen. Um das Enzym als Kern entstehen so Nanoschalen aus Zinkoxid. Sie haben einen einheitlichen äußeren Durchmesser von etwa 18 nm. Durch Verwendung von leicht veränderten Urease-Molekülen lässt sich die Größe der Zinkoxid-Schalen variieren.
Originalveröffentlichung: Hiroshi Matsui, Hunter College, City University of New York, "Urease as a Nanoreactor for Growing Crystalline ZnO Nanoshells at Room Temperature", Angewandte Chemie, 120, No. 29, 5495-5497 (2008).
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Forschung & Entwicklung

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.