Muschelfasern für die Bodenhaftung
Eisenatome verleihen Muschelfasern eine widerstandsfähige, aber dehnbare Beschichtung
Forscher am Max-Planck-Institut für Kolloid- und Grenzflächenforschung in Potsdam haben gemeinsam mit Kollegen aus Santa Barbara und Chicago herausgefunden, wie Muscheln ihre Haftfasern vor Abrieb schützen. Dafür verantwortlich ist eine Schutzschicht, die trotz ihrer Härte dennoch enorm dehnbar bleibt. Die Forscher entdeckten, dass die Proteinmatrix in dieser Schicht durch einzelne Eisenatome quervernetzt und damit verstärkt wird. Eine lokale Anhäufung dieser Vernetzungen bildet harte Kügelchen innerhalb der weichen und dehnbaren Schutzschicht. Dieses spezielle Design könnte neuartige abriebresistente, aber dehnbare Beschichtungen inspirieren.
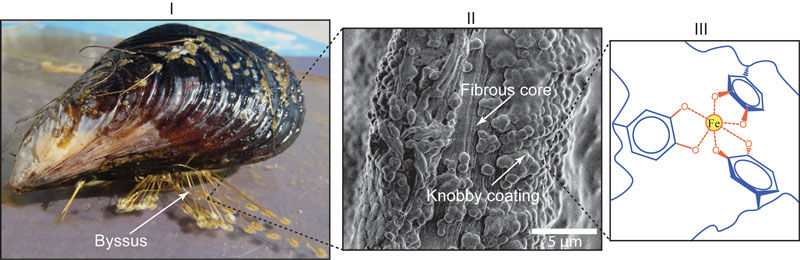
(I) Muscheln haften an harten Oberflächen (Küstenstreifen) mithilfe von Muschelseide (Byssus). (II) Dabei handelt es sich um dehnbare Fasern mit einer harten, rauen und schützenden Oberhaut (Elektronenmikroskopaufnahme). Die knubblige Oberfläche der Haut resultiert aus den körnigen Einschlüssen, die in eine deutlich weichere Matrix eingebettet sind. (III) Der Anteil von DOPA-Eisen-Komplexen ist in den harten Körnern sehr viel höher als in der umgebenden Matrix, welche die Dehnbarkeit gewährleistet.
Max-Planck-Gesellschaft
Muschelseide - ein Bündel von stabilen und dehnbaren Fasern
Muscheln haben sich in faszinierender Weise an eine besondere Form von Leben und Ernährung angepasst. Meist sind sie an Steinen oder Felsen festgeklebt, wo sie Nahrung aus dem Wasser filtern. Sie gedeihen gerade an den felsigen Küstenregionen und das trotz der extremen Umweltbedingungen. Einen großen Anteil daran hat die evolutionäre Entwicklung der Byssus, auch Muschelseide genannt.
Meermuscheln benutzen Muschelseide - ein Bündel von stabilen und dehnbaren Fasern - um sich an die felsigen Küstenstreifen anzuheften, an die die Wellen branden. Die dehnbaren Fasern werden von einer dünnen, harten Oberhaut mit einem biologischen Polymer bedeckt, die an Sandpapier erinnert. Obwohl so hart wie etwa Epoxid, ist diese knubblige Oberhaut dennoch erstaunlich strapazierbar: Sogar bei hundertprozentiger Dehnung reißt oder bricht sie nicht. Die einzelnen Stränge der Byssus werden von der Muschel in einem Prozess, der dem Spritzgussverfahren ähnelt, gebildet. Sie sind dafür verantwortlich, dass sich die ungeheure Energie der Brandungswellen verteilt, und schützen die Muschel vor Abriebschäden durch Gestein und Geröll in den Wassermassen.
Außergewöhnliche Kombination von Härte und Dehnbarkeit
"Schutzbeschichtungen sind extrem wichtig für die Haltbarkeit von Materialien und Geräten. Betrachtet man die Kombination von Härte und Dehnbarkeit, so gibt es nur wenige Polymere oder Zusammensetzungen, die diese Materialeigenschaften vereinen. Zu verstehen, wie ein flexibles Substrat vor äußeren Einflüssen geschützt werden kann, wird heute immer wichtiger", erklärt Matthew Harrington, Humboldt-Stipendiat am Max-Planck-Institut für Kolloid- und Grenzflächenforschung. Die Oberhaut der "Muschelseide" hat eine sehr knubblige Anmutung. Sie entsteht durch weniger als ein Tausendstel Millimeter große Körnchen (Granula), die in eine deutlich weichere Matrix eingebettet sind. Wird die Matrix gedehnt, bilden sich winzige Hohlräume, die womöglich größere Risse und damit einen generellen Materialdefekt verhindern. Dabei spielen die hohe Konzentration von Eisen-Ionen und die ungewöhnliche Veränderung der Aminosäure Tyrosin, gemeinhin bekannt als L-DOPA, eine entscheidende Rolle.
L-DOPA findet man in hohen Konzentrationen in der Schutzschicht dieser Fasern, als Bestandteils des Muschelfußproteins (mfp-1). L-DOPA verbindet sich leicht mit Übergangsmetall-Ionen wie Eisen und unterscheidet sich dadurch von typischen Aminosäuren. Admir Masic, beteiligter Wissenschaftler erklärt: "Verbinden sich zwei bis drei L-DOPA mit nur einem einzigen Eisen-Ion, bilden sie einen unglaublich stabilen Komplex, der für die Vernetzung von Strukturproteinen eingesetzt werden kann." Diese Metallproteinkomplexe haben eine hohe Bruchfestigkeit und sind beinahe halb so stabil wie kovalente Bindungen). Aber im Gegensatz zu kovalenten Bindungen können diese Brüche rückgängig gemacht werden. Das macht sie ideal für die Bildung von Vernetzungen, die bei Belastung notfalls aufbrechen, um das Material vor größeren Beschädigungen zu schützen.
Muschelhaut wird durch DOPA-Eisen-Komplexe stabilisiert
Die Forscher benutzten die konfokale Raman-Spektroskopie, um die chemische Zusammensetzung der Oberhaut zu erforschen. Darunter versteht man eine spektroskopische Untersuchung der inelastischen Streuung von Licht an Molekülen oder Festkörpern, die unter anderem für die Untersuchung von Materialeigenschaften eingesetzt wird. Mit dieser Methode konnten die Wissenschaftler den ersten direkten Beweis liefern, dass die Haut aus einem polymeren Proteingerüst besteht, welches durch DOPA-Eisen-Komplexe stabilisiert wird. Darüber hinaus entdeckten sie, dass die Verteilung von DOPA-Eisen-Komplexen in den Bereichen niedrig ist, in denen es granuläre Einschlüsse gibt, bzw. dort hoch ist, wo diese nicht existieren. Zusammen mit früheren mechanischen Beobachtungen lassen diese Ergebnisse vermuten, dass die eng vernetzten Granulate als stabilisierende Einschlüsse fungieren, während die weniger vernetzte Matrix jederzeit aufgebrochen werden kann und sich somit dehnen lässt.
"Die Natur hat eine elegante Methode für ein Problem entwickelt, mit der Ingenieure noch immer kämpfen: Sie hat Eigenschaften, die einen Abrieb verhindern und dennoch eine hohe Dehnbarkeit gewährleisten, in einem Material vereinigt", sagt Peter Fratzl, Direktor der Abteilung Biomaterialien am Max-Planck-Institut für Kolloid- und Grenzflächenforschung und ebenfalls an dieser Forschung beteiligt. Offensichtlich erreicht die Schutzschicht der Muschelseide dies durch eine sorgfältige, maßgeschneiderte Verbindung von Metall und Protein. "Es ist denkbar, dass ähnliche Strategien auf technisch entwickelte Polymerschutzschichten angewendet werden können."
Originalveröffentlichung: Matthew J. Harrington, Admir Masic, Niels Holten-Andersen, J. Herbert Waite, and Peter Fratzl; "Iron-clad fibers: a metal-based biological strategy for hard flexible coatings"; Science 2010.
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!