Meilenstein in der Biokatalyse-Forschung
TU Graz-Forschenden gelang es erstmals ein Enzym so „umzuschulen“, dass es statt seiner natürlichen Aufgabe Doppelbindungen zu reduzieren, nun ringförmige Molekülgerüste aufbaut. Die Arbeit mit Relevanz für die Produktion von Medikamenten oder Pflanzenschutzmitteln wurde in Angewandte Chemie publiziert.

Kathrin Heckenbichler und Rolf Breinbauer setzen mit ihrem Team Meilenstein in der Biokatalyse-Forschung
© TU Graz
Die Biokatalyse setzt Enzyme ein um chemische Reaktionen herbeizuführen. Vielfach ersetzt diese „sanfte Chemie“ dabei die Verwendung giftiger Reagenzien oder Lösungsmittel in bereits bestehenden Synthesen. Eine große Herausforderung für die Biokatalyse ist es jedoch dieses elegante Konzept auf völlig neuartige chemische Reaktionen zu übertragen, die für Enzyme aus der Natur unbekannt sind. Ein solch neues Design gelang nun einem Forschenden-Team an der TU Graz rund um Rolf Breinbauer, Leiter des Instituts für Organische Chemie, und Kathrin Heckenbichler, die diese Forschungsarbeit im Rahmen ihrer Dissertation am Institut für Organische Chemie der TU Graz betrieb. Breinbauer erklärt: „Es ist uns erstmals gelungen, ein Enzym so zu manipulieren, dass es statt seiner natürlichen Funktion nun eine unnatürliche, aber synthetisch noch viel interessantere Funktion erfüllt. Statt nämlich im katalytischen Prozess Doppelbindungen zu reduzieren, baut das Enzym nun Molekülgerüste in Form von kleinen Ringen auf. Durch den Austausch von nur einer Aminosäure im aktiven Zentrum des Enzyms gelang es uns, die natürliche Reaktion zu unterdrücken um einen neuen Reaktionsverlauf zu ermöglichen.“
Das Team rund um Heckenbichler und Breinbauer konnte erstmals mittels Biokatalyse sogenannte "Cyclopropane" erzeugen, das sind kleinstmögliche ringförmige organische Moleküle in der geometrischen Form eines Triangels. Solche Ringsysteme, auch Dreiringe genannt, kommen nicht nur in vielen Biomolekülen vor, sie sind auch ein wichtiges Strukturelement in Pflanzenschutzmitteln oder Pharmazeutika wie Antibabypillen, Asthma- oder AIDS-Medikamenten.
Die gute und die böse „Hand“ der Moleküle
Parallel gelang es den Forschenden auch, die Chiralität des erzeugten Moleküls zu beherrschen, was gerade bei der Herstellung von Medikamenten von großer Bedeutung ist. Chiralität oder auch „Händigkeit“ von Molekülen beschreibt die Tatsache, dass zwei Moleküle aus denselben Atomen, aber spiegelverkehrt aufgebaut sein können – gleich der rechten und der linken Hand. Von diesen sogenannten Enantiomeren kann eine Variante nützlich und die andere schädlich sein und es wird in der Herstellung von Medikamenten heute großer Wert darauf gelegt, nur die kurative Variante einzusetzen. So stellt man sicher, dass Medikamente sehr spezifisch wirken und durch den „chiralen Zwilling“ keine ungewollten Nebenwirkungen entstehen. Kathrin Heckenbichler erläutert Prozess und Ergebnis der biokatalytischen Umsetzung des Substrats: „Um eine optimale chirale Erkennung zwischen dem Enzym und Substrat zu ermöglichen, designten wir ein Substrat mit einem großen Rest. Dadurch gelang es uns, die räumlichen Bedingungen im aktiven Zentrum des Enzymes ideal auszunützen, um ein Cyclopropan in hoher Enantiomerenreinheit herzustellen.“ Den Forschenden gelang es so, von zwei möglichen chiralen Dreiringen nur das erwünschte Enantiomer herzustellen.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
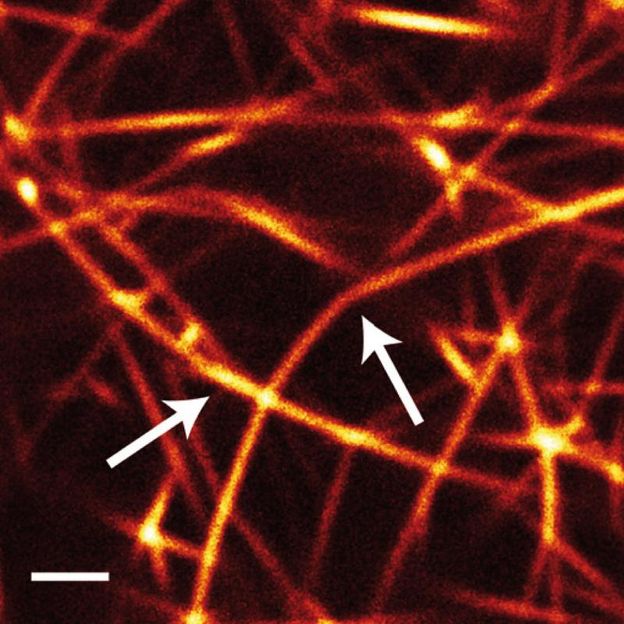
Modellsystem führt auf die Spur von Alterungsprozessen elastischer Polymere
Mesomerie
Millersche_Indizes
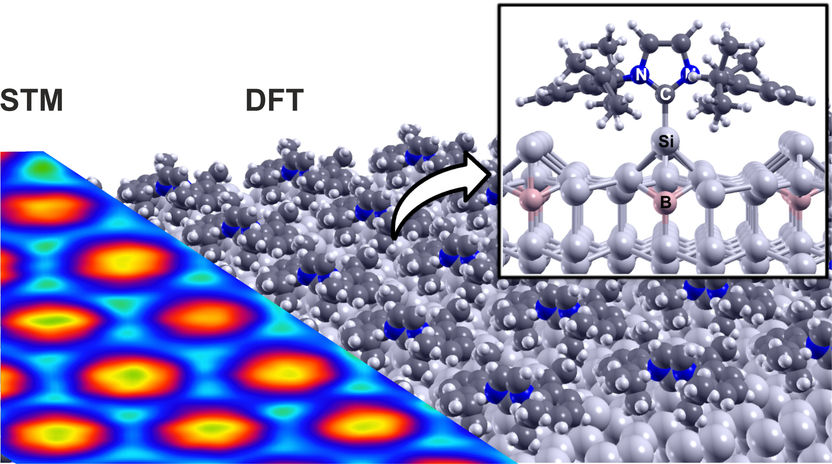
Neues Verfahren zur molekularen Funktionalisierung von Oberflächen - Stabile und geordnete Molekül-Einzellagen auf Silizium durch Selbstorganisation

Hohe Qualität und technologischer Vorsprung: High-Tech Gründer zeigen sich in Bestform - Gewinner der Konzeptphase des Science4Life Venture Cup 2016 prämiert

Emerson Process Management - Austin, USA

Aparatos, S.A. de C.V. - México, D.F., Mexiko
Viruzid

Zehn Gründe für ein modernes ICP-OES für die Routine-Analytik - Moderne ICP-OES bieten eine uneingeschränkte Leistungsfähigkeit für eine Vielzahl von Anwendungen






























































