Was Lithium-Akkus explosiv macht
Neues Modell erklärt Dendritenwachstum in Batterien
Brennende Smartphones oder sogar Elektroautos sind nicht nur Gegenstand etlicher YouTube-Videos. Weltweit gehen Forschende den Auslösern solcher Batteriebrände nach. Dabei handelt es sich oftmals um astartige Auswüchse ("Dendriten"), die beim Aufladen der Akkus entstehen. Bisher war allerdings nicht bekannt, warum Metalle wie Lithium Dendriten bilden, Silber oder Kupfer hingegen nicht. Nun haben die Chemiker Prof. Wolfgang Schmickler und Dr. Elizabeth Santos von der Universität Ulm ein Modell auf atomarer Ebene entwickelt, das erklärt, wie und warum Dendriten entstehen.

Symbolbild
pixabay.com/Unsplash
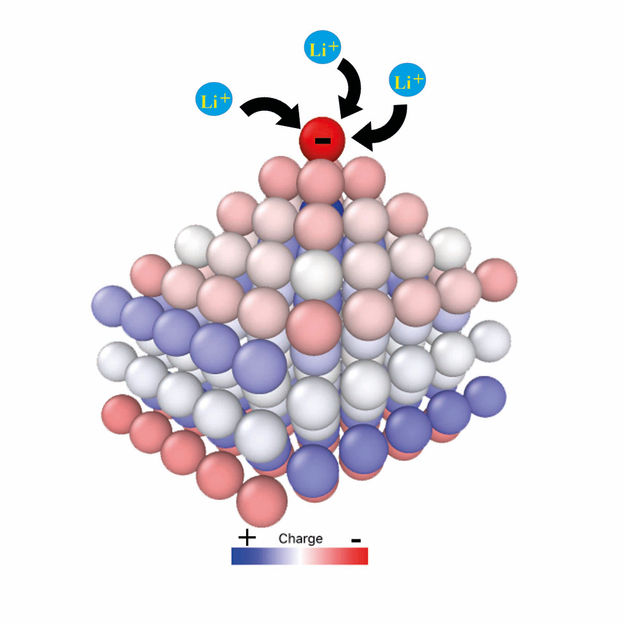
Schematische Darstellung der Dendritenbildung in einer Batterie: Die negative Ladung konzentriert sich auf den Spitzen von Vorsprüngen und zieht positiv geladene Lithium-Ionen an. Dadurch wachsen Dendriten heran
Schmickler/Santos; Uni Ulm

Lithiumbasierte Batterien sind extrem leistungsfähig – und womöglich hochexplosiv! Beim wiederholten Aufladen eines solchen Akkus bilden sich eventuell so genannte Dendriten, die einen Kurzschluss auslösen können: die Batterie geht in Flammen auf. Jetzt haben Chemiker der Universität Ulm ein Modell entwickelt, das erklärt, wie und warum bestimmte Metalle bei der Abscheidung Dendriten bilden. Dieser für die Batterieforschung bedeutende wissenschaftliche Beitrag ist als „Hot paper“ in der Fachzeitschrift „Angewandte Chemie“ erschienen.
Um die Energiewende zu meistern und die Elektromobilität voranzubringen, braucht die Welt neue, hochleistungsfähige Batterien. Bisher treiben vor allem Lithium-Ionen-Akkus Smartphones, Laptops oder Elektroautos an. Doch gerade für die Anforderungen der Elektromobilität ist die Leistungsfähigkeit dieser Batterien begrenzt. Das Problem: Um Kurzschlüsse zu vermeiden, sind Lithium-Ionen in Graphit eingelagert, was das Volumen und Gewicht der Akkus erhöht – und die Reichweite entsprechend sinken lässt. Batterien mit einer reinen Lithium-Elektrode hätten zwar eine deutlich höhere Energiedichte, neigen jedoch zur Dendritenbildung. Diese astartigen Auswüchse entstehen allmählich beim Aufladen der Batterie an der negativen Elektrode. Wenn sie die Gegenelektrode erreichen, können diese Dendriten im Zusammenspiel mit entflammbaren Elektrolyten einen Kurzschluss verursachen – die Batterie brennt ab. Mit diesem Phänomen beschäftigen sich nicht nur YouTube-Videos, sondern Forschende weltweit. Bisher ist allerdings noch nicht verstanden, warum Metalle wie Lithium Dendriten bilden, Kupfer oder beispielsweise Silber jedoch nicht. Weitere Materialien formieren die gefährlichen Kristallstrukturen erst bei sehr großer Spannung. Doch jetzt haben Professor Wolfgang Schmickler und Dr. Elizabeth Santos vom Institut für Theoretische Chemie der Universität Ulm ein Modell entwickelt, das die Entstehung der astartigen Dendriten erklärt.
Auf dem Ulmer Supercomputer JUSTUS 2 haben die Forschenden quantenchemische Berechnungen mithilfe einer Weiterentwicklung der Density-functional theory (DFBT+) durchgeführt. Ihre Ergebnisse legen folgendes Szenario für die Dendritenbildung nahe: Jedes Metall verfügt über einen so genannten Ladungsnullpunkt. Wird das Metall bei Potentialen unterhalb dieses Ladungsnullpunkts – also bei einer negativ geladenen Elektrode – abgeschieden, entstehen die kristallartigen Dendriten. „Bei der Abscheidung bilden sich immer wieder kleine Unebenheiten wie Vorsprünge auf der Oberfläche. Den Gesetzen der Elektrostatik folgend, konzentriert sich die negative Ladung auf den Spitzen solcher Cluster und zieht die positiv geladenen Lithium-Ionen an. Somit wachsen diese Spitzen weiter und bilden schließlich Dendriten“, erklärt Professor Schmickler. Darüber hinaus konnten die Forschenden ein weiteres Phänomen nachweisen, das zur Dendritenbildung beiträgt: Die negative Ladung verkleinert die Oberflächenspannung und fördert damit die Entstehung von Vorsprüngen auf der Oberfläche. Santos und Schmickler vergleichen diesen Vorgang mit Spülmittel, das die Bildung von Blasen im Wasser erleichtert.
Diese Erkenntnisse sind kompatibel mit bisherigen Forschungsergebnissen. Allerdings haben Schmickler und Santos mit ihren Berechnungen erstmals ein Modell auf atomarer Ebene entwickelt. Dieses lässt sich auf andere Metalle übertragen und erklärt gleichzeitig, warum beispielsweise Kupfer keineswegs anfällig für Dendriten ist. „Bei Metallen wie Kupfer oder Silber ist die Oberfläche bei der Abscheidung positiv geladen. Bildet sich dort ein kleiner Vorsprung auf der Oberfläche, sammelt sich eine positive Ladung an. Diese stößt die positiv geladenen Metall-Ionen ab, das Cluster kann nicht weiter wachsen und Dendriten bilden“, erläutert Dr. Elizabeth Santos.
Welche praktische Relevanz haben diese Forschungsergebnisse für die Entwicklung hochleistungsfähiger Batterien? Mit ihrem neuen Modell können die Chemiker zeigen, warum einige relevante Materialien Dendriten bilden und andere nicht. Darüber hinaus liefern sie eine Erklärung für die Entstehung der Kristallstrukturen auf atomarer Ebene. „Im Prinzip sagt unser Modell voraus, wie sich die Bildung von Dendriten in aufladbaren Batterien vermeiden lässt. Hierfür wäre allerdings ein Lösungsmittel erforderlich, das widersprüchliche Anforderungen erfüllt. Daher haben unsere Ergebnisse zunächst vor allem theoretische Relevanz“, betonen die Autoren.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.

Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.






























































