Warum 2D-Materialien schmelzen, wenn es kalt wird
„Dass Moleküle durch Kühlen mobil werden, scheint zunächst paradox – normalerweise passiert das durch Erwärmen“
Das Eis am Stiel in der Sommerhitze, der zugefrorene See im Frühling – üblicherweise schmelzen Materialien, wenn sie wärmer werden. Dabei werden kleine Teilchen wie Atome und Moleküle mobil: Sie sind nicht mehr an einem festen Ort verankert, sondern können sich ungeordnet bewegen. Wissenschaftler der Fakultät für Chemie der Universität Bielefeld haben nun gezeigt, dass dieser Prozess auch umgekehrt funktioniert: Molybdänacetat-Moleküle, die bei Zimmertemperatur eine geordnete Struktur auf der Oberfläche von Kupfer bilden, werden nicht durch Erwärmen, sondern durch Kühlen mobil.

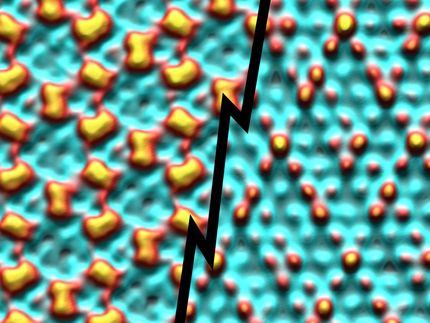
Aufnahmen mit dem Rastertunnelmikroskop zeigen, wie Molybdänacetat-Moleküle mobil werden: Bei 300 Kelvin (ca. 27 °C, li.) sind die Moleküle geordnet. Bei 220 Kelvin (ca. -53 °C, re.) löst sich die Kettenstruktur teilweise auf.
Universität Bielefeld/A. Kühnle
Ihre Ergebnisse präsentieren die Forschenden im Fachmagazin Angewandte Chemie. Die Arbeit ist in Kooperation mit Forschenden der Universitäten Mainz und Kaiserslautern entstanden.
„Dass Moleküle durch Kühlen mobil werden, scheint zunächst paradox – normalerweise passiert das durch Erwärmen“, sagt Professorin Dr. Angelika Kühnle, die die Arbeitsgruppe Physikalische Chemie I an der Fakultät für Chemie leitet. Tatsächlich wurde der umgekehrte Vorgang aber schon lange vorhergesagt. „Bereits 1903 hat Gustav Tammann, Chemiker an der Universität Göttingen, über diesen Vorgang spekuliert und ihn ‚inverses Schmelzen‘ genannt.“ Bisher wurde inverses Schmelzen nur in speziellen Situationen beobachtet: zum Beispiel unter extremen Bedingungen wie hohem Druck oder für besondere Materialien wie Helium. Andere Materialien, etwa Metalllegierungen, können durch Kühlen zwar von einem geordneten in einen ungeordneten Zustand übergehen – wie beim Schmelzen –, die Teilchen werden jedoch nicht mobil.
„Wir zeigen, dass Moleküle durch Kühlen nicht nur ungeordnet, sondern tatsächlich mobil werden können“, sagt Kühnle. Dazu verwenden die Wissenschaftler die Verbindung Molybdänacetat. Bei Zimmertemperatur bilden Molybdänacetat-Moleküle, die in einer einlagigen Schicht auf einer Kupferoberfläche aufgebracht werden, eine geordnete Struktur. Solche zweidimensionalen Systeme haben auch andere Forschende schon untersucht. Sie konnten die Mobilisierung der Moleküle aber nicht eindeutig nachweisen. Dies ist Kühnles Team in Zusammenarbeit mit Forschenden der Johannes Gutenberg-Universität Mainz und der Technischen Universität Kaiserslautern nun gelungen. „Weil strenggenommen nur dreidimensionale Materialien schmelzen können, nennen wir den Vorgang Mobilisierung durch Kühlen“, sagt Kühnle.
Bei minus 50 Grad werden die Molybdänacetat-Moleküle mobil
„Für unsere Studie haben wir das System aus Kupfer und Molybdänacetat auf ungefähr minus 50 Grad Celsius gekühlt. Dabei konnten wir beobachten, dass sich die geordnete Struktur auflöst und die Molybdänacetat-Moleküle mobil werden“, sagt Dr. Simon Aeschlimann, der in Kühnles Arbeitsgruppe geforscht hat und Erstautor der veröffentlichten Studie ist. Bei Zimmertemperatur stehen die Molybdänacetat-Moleküle aufrecht und reihen sich in Ketten aneinander. Bei minus 50 Grad Celsius zerfällt diese Kettenstruktur in einigen Bereichen: Moleküle lösen sich von den Enden der Ketten ab und lagern sich an einer anderen Stelle wieder an, oder bilden nur noch einzelne gekrümmte Ketten.
Die Voraussetzung dafür, dass ein System durch Kühlen von einer geordneten in eine mobile Phase übergeht, ist eine Verringerung der Entropie. Die Entropie ist ein Maß für die Anordnungs- und Bewegungsmöglichkeiten, die Atome oder Moleküle in einem System haben. Normalerweise nimmt die Entropie zu, wenn sich eine geordnete Struktur auflöst, weil die einzelnen Teilchen mehr Möglichkeiten haben: Sie können sich zum Beispiel in verschiedenen Richtungen bewegen, statt einen festen Platz einzunehmen. „Das passiert üblicherweise beim Schmelzen, etwa bei Metallen: Die geordnete Struktur löst sich auf, die Metallatome können sich hin und her bewegen und die Entropie des Systems steigt“, sagt Kühnle.
Im Molybdänacetat-Kupfer-System tragen jedoch nicht nur die Möglichkeiten, sich in die verschiedenen Raumrichtungen zu bewegen, zur Entropie bei. „Ein Molybdänacetat-Molekül, das in einer Kettenstruktur angeordnet ist, hat zwar keine Möglichkeit, seinen Platz zu verlassen. Aber weil es aufrecht steht und nicht so stark an die Kupferoberfläche gebunden ist, hat es die Möglichkeit, bestimmte Teile von sich zu bewegen – als würde es mit den Ohren wackeln“, sagt Kühnle. In der ungeordneten Phase liegen die Molybdänacetat-Moleküle hingegen flach auf der Oberfläche und sind stärker gebunden. „Jetzt kann das Molekül, um im Bild zu bleiben, auf dem Bauch liegend hin und her robben, aber es kann nicht mehr mit den Ohren wackeln“, so Kühnle. Deswegen nimmt die Entropie des Systems ab, obwohl es in eine mobile Phase übergeht.
Ein Rastertunnelmikroskop erzeugt Bilder der Oberflächenstruktur
Für ihre Untersuchung haben die Wissenschaftler ein Rastertunnelmikroskop genutzt. „Bei der Rastertunnelmikroskopie wird eine winzig kleine Nadel über die Materialien bewegt und der Strom zwischen Nadelspitze und Oberfläche gemessen. Dies erzeugt dann ein Bild der Oberflächenstruktur“, sagt Aeschlimann. Auf den Aufnahmen, die er mit seinen Kolleg*innen erstellt hat, ist erkennbar, dass bei niedrigeren Temperaturen ungeordnete, flockige Bereiche statt einer durchgehenden Kettenstruktur entstehen. Mit Computersimulationen haben die Forschenden diese Untersuchung ergänzt.
Die Wissenschaftler wollen mit ihrer Studie, die das Fachmagazin als besonders wichtige Veröffentlichung eingestuft hat, in erster Linie dazu beitragen, zweidimensionale Systeme und inverse Schmelzvorgänge besser zu verstehen. „Phasenübergänge haben aber häufig auch einen praktischen Nutzen – zum Beispiel wenn Eiswürfel Getränke kühlen oder Latentwärmespeicher Häuser isolieren. Auch für solche Anwendungen sind unsere Forschungen relevant“, so Kühnle.