Birnessit-Studie bietet Erkenntnisse für Elektrochemie und Energiespeicherung
Die Adsorption von Ionen aus dem Elektrolyten an einer Elektrodenoberfläche ist ein allgegenwärtiger Prozess, der sowohl für bestehende als auch für neue elektrochemische Energietechnologien genutzt wird. Aber was passiert, wenn diese Ionen in sehr kleine Räume eindringen? Um dieser Frage nachzugehen, untersuchten Forscher der NC State University das Verhalten eines "klassischen" Materials, Birnessit.
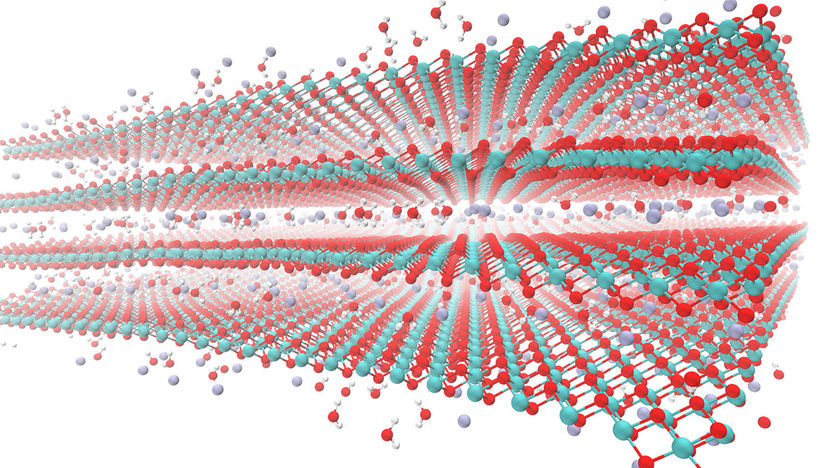
Dieses Bild zeigt das Material Birnessit mit Wassermolekülen (roter Sauerstoff, zwei weiße Wasserstoffmoleküle) und Kaliumkationen (dunkelblau/lavendel) an den Außenflächen und in der Zwischenschicht.
Karthik Ganeshan
Birnessit ist eine hydratisierte, geschichtete Form von Manganoxid, die über viele Zyklen hinweg eine Vielzahl positiver Ionen aus Elektrolyten speichern und wieder abgeben kann. Dies macht es vielversprechend für den Einsatz in elektrochemischen Hochleistungs-Energiespeichern oder in neuen elektrochemischen Technologien wie der Entsalzung und der Rückgewinnung seltener Elemente aus Wasser. Darüber hinaus ist es ein reichlich vorhandenes Material, das leicht herzustellen und ungiftig ist.
Der Mechanismus, durch den Birnessit Kationen aufnehmen und abgeben kann, wurde sowohl als faradaisch (mit Ladungstransfer) als auch als nicht-faradaisch (nur mit elektrostatischer Ionenadsorption) beschrieben.
Um diese Debatte zu klären, verwendeten die Forscher sowohl experimentelle als auch rechnerische Ansätze.
"In der Energiespeichergemeinde denken wir normalerweise, dass Ladungsspeicherung entweder faradaisch oder nicht-faradaisch ist", sagt Shelby Boyd, Erstautorin eines Artikels über die Arbeit und Postdoktorandin an der North Carolina State University. "An planaren Grenzflächen bezieht sich faradaisch auf die spezifische Adsorption eines Ions an einer Elektrode mit entsprechendem Ladungstransfer, wie bei einer Redoxreaktion. Als nicht-faradaisch bezeichnet man die rein elektrostatische Adsorption ohne Ladungstransfer. Bisher wurden diese Mechanismen der Ladungsspeicherung weitgehend als sich gegenseitig ausschließend dargestellt. Bei Birnessit haben wir jedoch festgestellt, dass das strukturelle Wasser in der Nanokonzentration der Zwischenschicht die Wechselwirkungen zwischen dem interkalierten Kation und dem Birnessit abschwächt. Dies führt zu einem Zwischenverhalten zwischen den beiden Arten von Adsorptionsextremen an planaren Grenzflächen.
Die Forscher konnten außerdem experimentell und theoretisch nachweisen, dass das Wasser zwischen den Schichten des Birnessits effektiv als Puffer dient, der kapazitives Verhalten ermöglicht, ohne eine signifikante strukturelle Veränderung des Birnessits zu verursachen.
Letztendlich, so die Forscher, zeigen die Ergebnisse zwei zukünftige Richtungen für die Arbeit auf, die beide für das breitere Feld der Elektrochemie vielversprechend sind.
"Das Gebiet der Elektrochemie erlebt derzeit eine Renaissance", sagt Veronica Augustyn, korrespondierende Autorin der Studie und Assistenzprofessorin für Materialwissenschaften und Ingenieurwesen an der NC State. "Die Möglichkeit, experimentelle Ergebnisse mit der Modellierung der elektrochemischen Grenzfläche auf atomarer Ebene zu verbinden, erlaubt es uns, tiefer als je zuvor zu bohren und Fragen zu stellen wie: Welche Rolle spielt das Lösungsmittel? Was könnte passieren, wenn die Reaktion unter Einschluss stattfindet? Indem wir den kapazitiven Mechanismus eines Materials wie Birnessit verstehen, schaffen wir die Voraussetzungen für das Verständnis komplexerer elektrochemischer Reaktionen."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.

Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.























































