Zwei sind besser als einer: Einatomiger Dimer-Elektrokatalysator für die grüne Wasserstoffproduktion
Nickel-Kobalt-Metalldimer auf stickstoffdotiertem Kohlenstoff kann die Elektrolyse sowohl unter sauren als auch unter basischen Bedingungen katalysieren
Die begrenzten Vorräte an fossilen Brennstoffen und die zunehmende Bedrohung durch den Klimawandel haben Forscher dazu veranlasst, alternative Technologien zur Herstellung umweltfreundlicher Brennstoffe zu entwickeln. grüner Wasserstoff, der durch Elektrolyse von Wasser mit Hilfe von erneuerbarem Strom erzeugt wird, gilt als erneuerbare Energiequelle der nächsten Generation für die Zukunft. Aufgrund der hohen Kosten der Elektrolyse wird der überwiegende Teil des Wasserstoffs jedoch aus der Raffination fossiler Brennstoffe gewonnen.
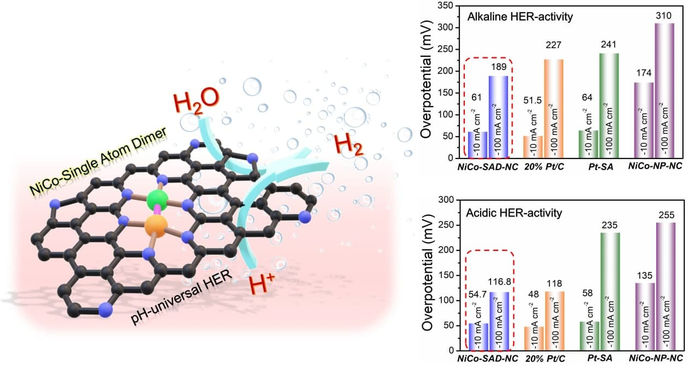
Schematische Darstellung der Wasserstoffentwicklungsreaktion (HER) mit NiCo-SAD, stabilisiert auf N-dotiertem Kohlenstoff (links). HER-Aktivität in alkalischen (oben rechts) und sauren Medien (unten rechts).
Institute for Basic Science
Derzeit ist die Effizienz der Wasserelektrolyse begrenzt und erfordert oft eine hohe Zellspannung, da es an effizienten Elektrokatalysatoren für die Wasserstoffentwicklung fehlt. Edelmetalle wie Platin (Pt) werden als Katalysatoren verwendet, um die Wasserstofferzeugung sowohl in sauren als auch in alkalischen Medien zu verbessern. Diese Edelmetallkatalysatoren sind jedoch sehr teuer und weisen eine schlechte Stabilität im Langzeitbetrieb auf.
In jüngster Zeit haben Einzelatomkatalysatoren im Vergleich zu ihren auf Nanomaterialien basierenden Pendants eine hervorragende Aktivität gezeigt. Dies liegt daran, dass sie eine Atomausnutzung von bis zu 100% erreichen können, während bei Nanopartikeln nur die Oberflächenatome für die Reaktion zur Verfügung stehen. Aufgrund der Einfachheit des Ein-Atom-Zentrums ist eine weitere Modifizierung der Katalysatoren zur Durchführung komplexer mehrstufiger Reaktionen jedoch recht schwierig.
Der einfachste Weg, die einzelnen Atome zu modifizieren, besteht darin, sie in einatomige Dimere zu verwandeln, die zwei verschiedene einzelne Atome miteinander verbinden. Die Abstimmung des aktiven Zentrums von Einzelatomkatalysatoren mit Dimeren kann die Reaktionskinetik dank des synergistischen Effekts zwischen zwei verschiedenen Atomen verbessern. Während die Synthese und Identifizierung der einatomigen Dimerstruktur konzeptionell bekannt ist, war ihre praktische Umsetzung jedoch sehr schwierig.
Dieses Problem wurde von einem Forschungsteam unter der Leitung des stellvertretenden Direktors LEE Hyoyoung vom Center for Integrated Nanostructure Physics des Institute for Basic Science (IBS) an der Sungkyunkwan University angegangen. Das IBS-Forschungsteam entwickelte erfolgreich eine atomar dispergierte Ni-Co-Dimer-Struktur, die auf einem stickstoffdotierten Kohlenstoffträger stabilisiert ist und NiCo-SAD-NC genannt wurde.
"Wir synthetisierten eine Ni-Co-Einzelatom-Dimerstruktur auf einem Stickstoff (N)-dotierten Kohlenstoffträger durch In-situ-Einschluss von Ni/Co-Ionen in die Polydopamin-Kugel, gefolgt von einer Pyrolyse mit genau kontrollierter N-Koordination. Wir haben modernste Transmissionselektronenmikroskopie und Röntgenabsorptionsspektroskopie eingesetzt, um diese NiCo-SAD-Stellen mit atomarer Präzision zu identifizieren", sagt Ashwani Kumar, der Erstautor der Studie.
Die Forscher fanden heraus, dass eine zweistündige Glühung bei 800 °C in einer Argon-Atmosphäre die beste Bedingung für die Erzielung der Dimerstruktur war. Auch andere einatomige Dimere wie CoMn und CoFe konnten mit der gleichen Methode synthetisiert werden, was die Allgemeingültigkeit ihrer Strategie beweist.
Das Forscherteam bewertete die katalytische Effizienz dieses neuen Systems anhand des Überpotentials, das für die Wasserstoffentwicklungsreaktion erforderlich ist. Der NiCo-SAD-NC-Elektrokatalysator wies eine vergleichbare Überspannung auf wie kommerzielle Pt-basierte Katalysatoren in sauren und alkalischen Medien. NiCo-SAD-NC zeigte auch eine 8-mal höhere Aktivität als Ni/Co-Einzelatomkatalysatoren und heterogene NiCo-Nanopartikel in alkalischen Medien. Gleichzeitig erreichte er eine 17- bzw. 11-mal höhere Aktivität als Co- und Ni-Einzelatomkatalysatoren und eine 13-mal höhere Aktivität als herkömmliche Ni/Co-Nanopartikel in sauren Medien.
Darüber hinaus wiesen die Forscher die Langzeitstabilität des neuen Katalysators nach, der die Reaktion 50 Stunden lang ohne jegliche Strukturveränderung durchführen konnte. Die NiCo-SAD wies im Vergleich zu anderen einatomigen Dimeren und einatomigen Ni/Co-Stellen eine überlegene Wasserdissoziation und eine optimale Protonenadsorption auf, wodurch die Aktivität des pH-universellen Katalysators auf der Grundlage der Dichtefunktionaltheorie-Simulation erhöht wurde.
"Wir waren sehr erfreut zu entdecken, dass die neuartige NiCo-SAD-Struktur Wassermoleküle mit einer viel niedrigeren Energiebarriere dissoziiert und die Wasserstoffentwicklungsreaktion sowohl in alkalischen als auch in sauren Medien mit einer Leistung beschleunigt, die mit der von Pt vergleichbar ist, was die Unzulänglichkeiten der einzelnen einatomigen Ni- und Co-Katalysatoren beseitigt. Die Synthese einer solchen einatomigen Dimerstruktur war eine seit langem bestehende Herausforderung auf dem Gebiet der einatomigen Katalysatoren", erklärt Associate Director Lee, der korrespondierende Autor der Studie.
Er erklärt weiter: "Diese Studie bringt uns einen Schritt näher an eine kohlenstofffreie und grüne Wasserstoffwirtschaft. Dieser hocheffiziente und kostengünstige Elektrokatalysator für die Wasserstofferzeugung wird uns helfen, die langfristigen Herausforderungen einer wettbewerbsfähigen grünen Wasserstoffproduktion zu meistern: hochreiner Wasserstoff für kommerzielle Anwendungen zu einem niedrigen Preis und auf umweltfreundliche Weise zu produzieren."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.































































