Neue, nachhaltige Methode zur Herstellung von Wasserstoff für Brennstoffzellen und Düngemittel
„Wir haben etwas erreicht, was Wissenschaftlern jahrzehntelang verwehrt geblieben ist“
Ein neues nachhaltiges und praktisches Verfahren zur Herstellung von Wasserstoff aus Wasser wurde von einem Forschungsteam des RIKEN Center for Sustainable Resource Science (CSRS) in Japan unter der Leitung von Ryuhei Nakamura entdeckt. Im Gegensatz zu den derzeitigen Methoden erfordert die neue Methode keine seltenen Metalle, die teuer oder knapp sind. Stattdessen kann Wasserstoff für Brennstoffzellen und landwirtschaftliche Düngemittel nun mit Kobalt und Mangan, zwei relativ weit verbreiteten Metallen, hergestellt werden. Die Studie wurde in Nature Catalysis veröffentlicht.
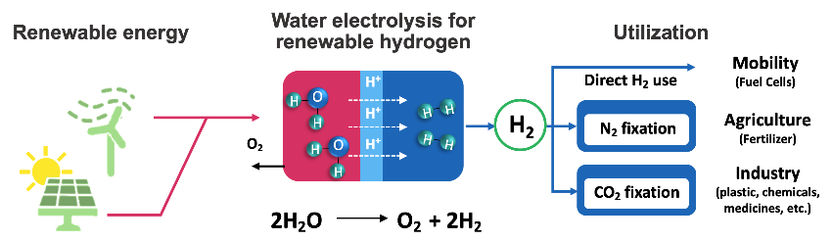
Dieses Schema zeigt das Konzept für eine nachhaltige Wasserstofferzeugung. Strom aus erneuerbaren Quellen (Sonne, Wind) wird verwendet, um Wasser in Sauerstoff und Wasserstoff zu spalten (Elektrolyse). Der Wasserstoff kann dann als Kraftstoff, zur Herstellung von Dünger aus Ammoniak und in anderen Industriezweigen, verwendet werden.
RIKEN

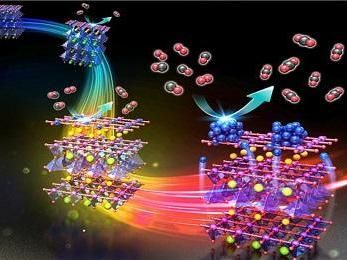
(Links) Das Kobalt-Mangan-Mischoxid, Co2MnO4. (Rechts) Ein Bild aus einem Video, das die Herstellung von Wasserstoff durch Elektrolyse bei einer Stromdichte von 1000 Milliampere pro Quadratzentimeter zeigt.
RIKEN

Im Gegensatz zu herkömmlichen fossilen Brennstoffen, bei deren Verbrennung Kohlendioxid entsteht, ist Wasserstoff ein sauberer Brennstoff, bei dem nur Wasser als Nebenprodukt anfällt. Wenn Wasserstoff mit Hilfe von erneuerbarem Strom aus Wasser gewonnen werden kann, kann das Energienetz sauber, erneuerbar und nachhaltig gestaltet werden. Darüber hinaus ist Wasserstoff der Hauptbestandteil, der zur Herstellung von Ammoniak benötigt wird, das in praktisch allen synthetischen Düngemitteln verwendet wird. Doch anstatt den Wasserstoff sauber aus Wasser zu gewinnen, verwenden Ammoniakwerke derzeit fossile Brennstoffe, um den benötigten Wasserstoff zu erzeugen.
Warum also verwenden wir immer noch fossile Brennstoffe? Ein Grund ist, dass das Verfahren zur Wasserstoffgewinnung selbst - die Elektrolyse - teuer und noch nicht nachhaltig ist.
„Das liegt vor allem daran, dass es an guten Katalysatoren mangelt“, sagt Nakamura. „Der Katalysator muss nicht nur in der Lage sein, der rauen sauren Umgebung standzuhalten, sondern auch sehr aktiv sein. Ist dies nicht der Fall, steigt die Menge an Strom, die für die Reaktion benötigt wird, um eine bestimmte Menge an Wasserstoff zu erzeugen, und damit auch die Kosten.“
Derzeit sind die aktivsten Katalysatoren für die Wasserelektrolyse seltene Metalle wie Platin und Iridium, was ein Dilemma darstellt, da sie teuer sind und als „gefährdete Spezies“ unter den Metallen gelten. Wollte man den gesamten Energiebedarf des Planeten auf Wasserstoff als Kraftstoff umstellen, würde dies, der heutigen Jahresproduktion von Iridium entsprechend, in etwa eine Produktionsmenge von 800 Jahren erfordern, eine Menge, die vielleicht gar nicht vorhanden ist. Andererseits sind häufig vorkommende Metalle wie Eisen und Nickel nicht aktiv genug und neigen dazu, sich in der rauen, sauren Elektrolyseumgebung sofort aufzulösen.
Auf der Suche nach einem besseren Katalysator untersuchten die Forscher eine Mischung aus Kobalt- und Manganoxiden. Kobaltoxide können für die erforderliche Reaktion aktiv sein, korrodieren aber sehr schnell in der sauren Umgebung. Manganoxide sind stabiler, aber nicht annähernd aktiv genug. Durch die Kombination der beiden Oxide hofften die Forscher, die Vorteile ihrer komplementären Eigenschaften nutzen zu können. Sie mussten auch die hohe Stromdichte berücksichtigen, die für eine praktische Anwendung außerhalb des Labors erforderlich ist. „Für die Wasserstoffproduktion im industriellen Maßstab mussten wir die Zielstromdichte unserer Studie auf das 10- bis 100-fache der in früheren Experimenten verwendeten Werte festlegen“, sagt Shuang Kong, Mitautor der Studie. „Die hohen Ströme führten zu einer Reihe von Problemen wie der physikalischen Zersetzung des Katalysators“.
Schließlich konnte das Team diese Probleme durch Versuch und Irrtum überwinden und entdeckte einen aktiven und stabilen Katalysator, indem es Mangan in das Spinellgitter von Co3O4 einfügte und so das gemischte Kobalt-Mangan-Oxid Co2MnO4 erzeugte.
Die Tests zeigten, dass Co2MnO4 sehr gut funktioniert. Die Aktivierungsniveaus lagen nahe an denen von Iridiumoxiden, die dem Stand der Technik entsprechen. Außerdem hielt der neue Katalysator über zwei Monate bei einer Stromdichte von 200 Milliampere pro Quadratzentimeter, was ihn für den praktischen Einsatz geeignet machen könnte. Im Vergleich zu anderen Katalysatoren aus Nicht-Seltenen Metallen, die in der Regel nur Tage oder Wochen bei viel niedrigeren Stromdichten halten, könnte der neue Elektrokatalysator einen Wendepunkt darstellen.
„Wir haben etwas erreicht, was Wissenschaftlern jahrzehntelang verwehrt geblieben ist“, sagt Co-Erstautor Ailong Li. „Die Wasserstoffproduktion mit einem hochaktiven und stabilen Katalysator, der aus reichlich vorhandenen Metallen besteht. Langfristig glauben wir, dass dies ein großer Schritt auf dem Weg zu einer nachhaltigen Wasserstoffwirtschaft ist. Wie bei anderen erneuerbaren Technologien wie Solarzellen und Windkraft erwarten wir, dass die Kosten der grünen Wasserstofftechnologie in naher Zukunft mit weiteren Fortschritten sinken werden.“
Der nächste Schritt im Labor wird darin bestehen, Wege zu finden, um die Lebensdauer des neuen Katalysators zu verlängern und seine Aktivität noch weiter zu erhöhen. „Es gibt immer Raum für Verbesserungen“, sagt Nakamura, „und wir streben weiterhin nach einem Katalysator ohne Seltene Metalle, der die Leistung der derzeitigen Iridium- und Platinkatalysatoren erreicht.“
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.