Das Platin-Rätsel
Wie eine chemische Reaktion abläuft, die nach bisheriger Sichtweise bei den beobachteten Temperaturen gar nicht möglich sein sollte
Was passiert, wenn eine Katze auf eine Sonnenblume klettert? Die Sonnenblume ist nicht stabil, sie wird sich rasch nach unten verbiegen, und die Katze ist wieder auf dem Boden. Wenn die Katze aber nur einen raschen Zwischenschritt benötigt, um von dort aus einen Vogel zu erwischen, dann kann die Sonnenblume als „metastabiler Zwischenschritt“ den entscheidenden Unterschied machen. Genau diesen Mechanismus kann man beobachten, wenn einzelne Atome eines Katalysators Moleküle einfangen, um sie dann chemisch umzuwandeln.
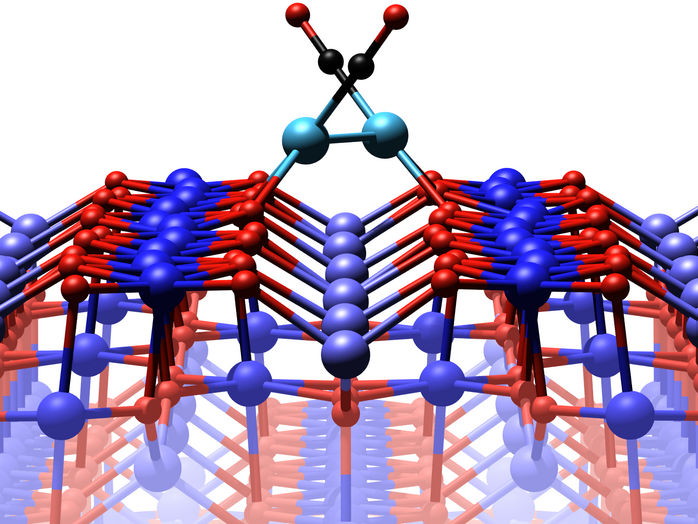
Die Eisenoxid-Oberfläche mit zwei Platin-Atomen, an denen Kohlenmonoxid-Moleküle andocken.
Technische Universität Wien
Schon vor Jahren hatte man festgestellt, dass Platin-Katalysatoren, die man zur Oxidation von Kohlenmonoxid verwendet, bei Temperaturen aktiv sind, bei denen sie nach bisher gängiger Sichtweise eigentlich noch gar keinen Effekt zeigen dürften. Ein Forschungsteam der TU Wien konnte mit Hilfe von Mikroskop-Aufnahmen auf atomarer Skala und aufwändigen Computersimulationen nun zeigen: Das lässt sich erklären, wenn man berücksichtigt, dass sowohl der Katalysator selbst als auch das Material, auf dem er verankert ist, für kurze Zeit metastabile Zustände annehmen. Die Ergebnisse wurden nun im Fachjournal „Science Advances“ publiziert.
Einzelne Atome als Katalysatoren
In der Forschungsgruppe von Prof. Gareth Parkinson am Institut für Angewandte Physik der TU Wien untersucht man die kleinsten Katalysatoren, die überhaupt möglich sind: Einzelne Platin-Atome werden auf einer Eisenoxid-Oberfläche platziert. Sie kommen dann in Kontakt mit Gas, das Kohlenmonoxid enthält und wandeln das giftige Kohlenmonoxid in Kohlendioxid um.
„Dieser Vorgang ist technisch sehr wichtig, was dabei aber auf atomarer Ebene genau geschieht, war bisher nicht klar“, sagt Gareth Parkinson. „In unserer Forschungsgruppe untersuchen wir solche Prozesse auf verschiedene Arten: Einerseits erzeugen wir in einem Rastertunnelmikroskop extrem hochauflösende Bilder, auf denen man die Bewegung einzelner Atome studieren kann. Und andererseits analysieren wir den Vorgang mit Computersimulationen.“
Ob die Platin-Atome als Katalysator aktiv sind, hängt von der Temperatur ab. Im Experiment wird der Katalysator langsam und gleichmäßig erwärmt, bis die kritische Temperatur erreicht ist, und Kohlenmonoxid zu Kohlendioxid umgewandelt wird. Diese Schwelle liegt bei ungefähr 550 Kelvin (rund 277°C). „Das passte aber nicht zu unseren ursprünglichen Computersimulationen“, sagt Matthias Meier, der Erstautor der aktuellen Publikation. „Nach der Dichtefunktionaltheorie, die man normalerweise für solche Berechnungen verwendet, sollte der Prozess erst bei 800 Kelvin stattfinden. Wir wussten also: Irgendetwas Wichtiges hatte man hier bisher übersehen.“
Ein Kurzzeit-Zustand: Nicht stabil, aber wichtig
Mehrere Jahre hindurch sammelte das Team in verschiedenen anderen Forschungsprojekten umfangreiche Erfahrung mit ähnlichen Materialien, dadurch ergab sich Schritt für Schritt ein neues Bild: „Mit der Dichtefunktionaltheorie berechnet man normalerweise jenen Zustand des Systems, der die niedrigste Energie hat“, sagt Matthias Meier. „Das ist auch sinnvoll so, denn das ist der Zustand, den das System am häufigsten annimmt. Doch in unserem Fall gibt es einen zweiten Zustand, der eine zentrale Rolle spielt: Einen sogenannten metastabilen Zustand.“
Sowohl die Platin-Atome als auch die Eisenoxid-Oberfläche können zwischen unterschiedlichen Atomanordnungen hin- und her wechseln. Der Grundzustand, mit der niedrigsten Energie, ist stabil. Wenn das System in den metastabilen Zustand wechselt, kehrt es nach kurzer Zeit unweigerlich wieder in den Grundzustand zurück – wie die Katze, die auf einer instabilen Sonnenblume nach oben gelangen will. Doch bei der katalytischen Umwandlung von Kohlenmonoxid genügt es, dass sich das System für kurze Zeit im metastabilen Zustand befindet: So wie der Katze vielleicht ein kurzer Moment in einem wackeligen Kletterzustand genügen, um mit der Pfote einen Vogel zu erwischen, kann der Katalysator im metastabilen Zustand Kohlenmonoxid umwandeln.
Zwei Platin-Atome, die sich auf der Eisenoxid-Oberfläche gemeinsam genau an der richtigen Stelle anlagern, halten je ein Kohlenmonoxid-Molekül fest. Das Eisenoxid kann im metastabilen Zustand genau an dieser Stelle seine atomare Struktur ändern, es gibt ein Sauerstoffatom frei, das sich mit einem der Kohlenmonoxid-Moleküle zu Kohlendioxid verbindet, das dann augenblicklich davonfliegt – der Katalyseprozess ist somit abgeschlossen. „Wenn wir diese bisher nicht berücksichtigen Kurzzeit-Zustände in unsere Computersimulation mit einbauen, dann kommen wir genau auf das Ergebnis, das auch im Experiment gemessen wurde“, sagt Matthias Meier.
„Unser Forschungsergebnis zeigt, dass man in der Oberflächenphysik oft viel Erfahrung braucht“, sagt Gareth Parkinson. „Hätten wir nicht im Lauf der Jahre ganz unterschiedliche chemische Prozesse studiert, hätten wir dieses Rätsel wohl nie gelöst.“ In letzter Zeit wird auch künstliche Intelligenz mit großem Erfolg für die Analyse quantenchemischer Prozesse verwendet – doch in diesem Fall hätte das wohl keinen Erfolg gebracht, ist Parkinson überzeugt. Um auf kreative Lösungen außerhalb des bisher für möglich gehaltenen zu kommen, braucht man wohl doch den Menschen.