Brausepulver als umweltfreundlicher Wasserstoffspeicher
Kohlendioxid-neutrale Wasserstoffspeicherung mit einem Bicarbonat/Formiat-System
Als ein aussichtsreicher Energieträger für eine zukünftige nachhaltige Energiewirtschaft wird Wasserstoff diskutiert. Allerdings werden noch praktikable Lösungen für eine einfache und sichere Wasserstoffspeicherung gesucht. Trotz verschiedener Fortschritte konnte bisher jedoch keine allgemein anwendbare Lösung gefunden werden, die alle Vorgaben der Industrie erfüllt. Matthias Beller und sein Team vom Leibniz-Institut für Katalyse in Rostock stellen in der Zeitschrift Angewandte Chemie nun einen neuen Ansatz zur Wasserstoffspeicherung vor, der auf einfachen Salzen der Ameisensäure und der Kohlensäure basiert.
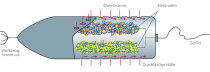
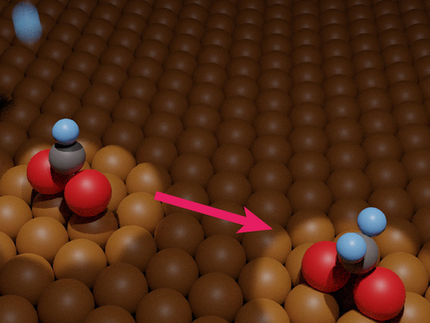
Praktikable Wasserstoffspeicher sollten den Wasserstoff bei Normaldruck und Raumtemperatur aufnehmen, eine hohe Menge sicher auf möglichst kleinem Raum unterbringen und ihn bei Bedarf unter den genannten Bedingungen rasch wieder abgeben können. Bekannte Metallhydrid-Tanks bringen den Wasserstoff sicher in einem relativ überschaubaren Volumen unter, sind jedoch sehr schwer, teuer und arbeiten nur bei höheren Temperaturen oder viel zu langsam. Neben organischen Wasserstoffspeichern wie Methan und Methanol interessiert sich die Forschung seit einiger Zeit für Ameisensäure (HCO2H) und ihre Salze, die so genannten Formiate, zur Wasserstofferzeugung. Ein grundlegendes Problem bei der Verwendung dieser Speichermaterialien ist die Abtrennung des bei der Wasserstoff-Freisetzung entstehenden Kohlendioxids. Dem Rostocker Team ist es nun gelungen, mit einem speziellen Ruthenium-Katalysator, der sowohl die Wasserstoff-Freisetzung als auch die Rückreaktion der Wasserstoffaufnahme katalysiert, einen reversiblen CO2-freien Wasserstoffspeicherzyklus zu etablieren. Konkret wird dabei Wasserstoff aus ungiftigen Formiaten freigesetzt und das entstehende CO2 in Form von Bicarbonaten abgefangen. Bicarbonate sind Bestandteil von vielen natürlichen Gesteinen und finden im Alltag auch Verwendung als Backpulver oder Brausepulver (Natriumbicarbonat, NaHCO3).
„Unser neues Konzept hat eine Reihe von Vorteilen“, sagt Beller, „verglichen mit CO2 ist festes Bicarbonat einfach zu handhaben und sehr gut in wässrigen Medien löslich. Die resultierende Bicarbonatlösung kann katalytisch unter sehr viel milderen Bedingungen in eine Formiatlösung überführt werden als man etwa für die Reaktionen zu Methan oder Methanol benötigt.“ Zudem könne der ungefährliche Feststoff einfach gelagert und transportiert werden. Die Wasserstoffentladung gelingt bereits bei Raumtemperatur oder auch darunter. Beller: „Vor allem aber wird erstmals ein geschlossener Kohlenstoffkreislauf möglich, da das resultierende Bicarbonat mit Wasserstoff einfach wieder aufgeladen werden kann.“
Originalveröffentlichung
Meistgelesene News
Originalveröffentlichung
Matthias Beller et al.; "Kohlenstoffdioxid-neutrale Wasserstoffspeicherung basierend auf Bicarbonaten und Formiaten"; Angewandte Chemie 2011
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte