Jacobs-Forscher weisen erstmals „biologische“ Halogenbindungen in künstlichem Molekülsystem nach
Wissenschaftler der Jacobs University identifizierten erstmals schwache chemische Wechselwirkungen in einem künstlichen Molekülsystem, wie sie bislang nur von biologischen Systemen, beispielsweise Proteinen, bekannt waren: Das Forscherteam konnte zeigen, dass Jod- bzw. Brom-Moleküle, die in das hohle, synthetische Container-Molekül Cucurbituril eingebracht wurden, über sogenannte perpendikulare Halogenbrücken in dem Molekülhohlraum gebunden wurden. Die Nutzung solcher biomimetischer Interaktionen in der Chemie eröffnet neue Entwicklungsmöglichkeiten für halogenhaltige Medikamente, Antiseptika, und Materialien für Batterien und Solarzellen.
Biomimetik – die Übertragung biologischer Funktionsprinzipien auf künstliche Systeme – basiert auf der These, dass sich in der Natur durch die Evolution optimierte Strukturen und Prozesse entwickelt haben und diese damit bestens als Vorbild für Lösungen in Technologie und Design geeignet sind. Während Biomimetik in der Technik weit verbreitet ist und in der Grundidee eine z. T. jahrhundertelange Tradition hat, ist die biomimetische bzw. bioinspirierte Chemie ein vergleichsweise junges Forschungsfeld, das erst seit den 1990er zunehmend an Bedeutung gewinnt. Biomimetische chemische Verbindungen gleichen in Bezug auf ihre funktionellen Eigenschaften biologischen Substanzen, sind oft jedoch stabiler als ihre natürlichen Vorbilder, da sie sich in ihrer Zusammensetzung deutlich von diesen unterscheiden. Bewährt haben sie sich daher vor allem zur Entwicklung künstlicher Modellsysteme, mit denen enzymatische, hormonelle und andere natürliche molekularbiologische Prozesse simuliert werden können, die nur schwer an lebenden Organismen oder in vitro mit natürlichen Systemen zu untersuchen sind.
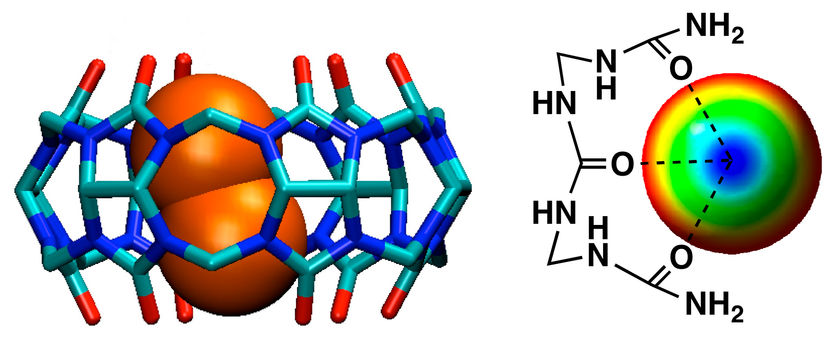
Unkonventionelle Bindung: Halogenmoleküle aus zwei Jod- oder Bromatomen (Grafik links, orange-braun), werden durch perpendikulare Halogenbrückenbindungen zu den Harnstoffgruppen im Hohlraum des synthetischen Container-Molekül Cucurbit[6]uril gebunden (Grafik rechts). Dieser Bindungstyp war bislang nur aus biologischen Systemen bekannt. Die Nutzung solcher biomimetischer Interaktionen in der Chemie eröffnet neue Entwicklungsmöglichkeiten für Medikamente- und Materialdesign.
An der Jacobs University wurde nun ein biomimetisches System entwickelt, in dem kleine Halogenmoleküle aus zwei Jod- bzw. Bromatomen sogenannte perpendikulare – also senkrechte – Halogenbrückenbindungen zu den Harnstoffgruppen eines hohlen Makromoleküls aus der Klasse der Cucurbiturile ausbildeten und so in dem Hohlraum des synthetischen, fassförmigen Containermoleküls gebunden wurden. Diese Art von schwacher chemischer Interaktion ist eine spezielle Form von Halogenbrücken, wie sie bislang nur aus der Biologie für halogenhaltige Proteinkomplexe bekannt waren. Das Forscherteam der Jacobs University konnte seine experimentellen Befunde durch Kristallstrukturen und mittels quantenchemischer Berechnungen verifizieren und damit erstmals diese „biologische“ Variante von Halogenbindungen für ein artifizielles Molekülsystem nachweisen.
„Durch die Übertragung der Halogenbrücken von Proteinen auf synthetische Moleküle ist es uns gelungen, die Triebkraft zur Ausbildung dieser ungewöhnlichen Bindungen nun wirklich im Detail zu verstehen und auch zu verallgemeinern. So ist es beispielsweise entscheidend, dass sowohl Proteine als auch Cucurbiturile Amidgruppen enthalten, und dass die Wechselwirkung in der Gegenwart von Wasser erfolgt“, sagt Werner Nau, Professor of Chemistry und Leiter der Studie. Mit seinem Team forscht er schwerpunktmäßig im Bereich der supramolekularen Chemie, die sich mit der Assoziation von Molekülen zu übergeordneten Strukturen befasst und den für diese Prozesse wichtigen schwachen Wechselwirkungen. Unterstützt wurde er von Ulrich Kortz, ebenfalls Chemieprofessor an der Bremer Privatuniversität, der mit seinem Team seine langjährige Expertise zur Strukturaufklärung komplexer molekularer Strukturen zu dem Kooperationsprojekt beisteuerte.
„Die beobachteten biomimetischen Wechselwirkungen erlauben aber nicht nur ein besseres Verständnis der Bindungen in biologischen Systemen, zum Beispiel für die Erkennung des Schilddrüsenhormons Thyroxin, sondern auch deren Nutzung für die Entwicklung neuer Materialien oder Pharmaka“, so Nau weiter. „Unsere Forschungsergebnisse liefern hier insofern neue Design-Kriterien, als bislang die von uns untersuchten schwachen Bindungskräfte bei der computergestützten Wirkstoffoptimierung vernachlässigt wurden“, so der Bremer Chemiker. „Das an das Cucurbituril komplexierte Jod erfährt zudem durch die biomimetischen Halogenbrücken eine besondere Stabilisierung, die für Anwendungen von großem Interesse ist. Das gebundene Jod ist in wässriger Lösung länger stabil, eine Eigenschaft, die wir zurzeit zur Entwicklung länger wirksamer jodhaltiger Antiseptika nutzen. Zudem untersuchen wir, ob durch Zugabe von Cucurbituril jodhaltige Herzschrittmacher-Batterien und organische Solarzellen in ihrer Leistung verbessert werden können, in denen Jod als Elektrodenmaterial dient“, so Jacobs-Professor Nau abschließend.
































































