Raumtemperatur-Umwandlung von CO₂ in CO: Ein neuer Weg zur Synthese von Kohlenwasserstoffen
Neue Methode könnte potenziell den Dioxidausstoß in die Atmosphäre reduzieren und die Kosten der chemischen Produktion senken
Forscher des National Institute of Standards and Technology (NIST) und ihre Kollegen haben eine Raumtemperaturmethode demonstriert, die den Kohlendioxidgehalt in den Abgasen fossiler Kraftwerke, eine der Hauptquellen für Kohlenstoffemissionen in der Atmosphäre, erheblich reduzieren könnte.
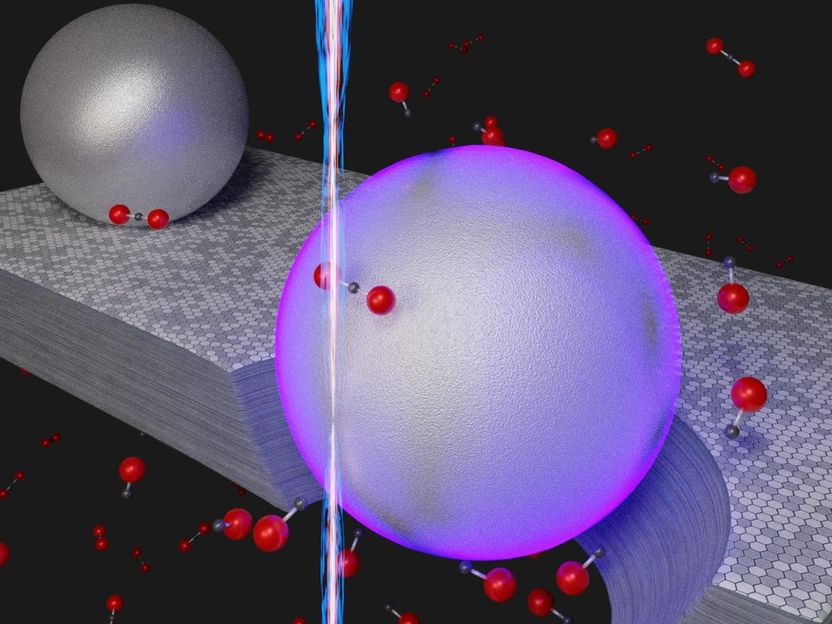
Illustration eines neuartigen Raumtemperaturverfahrens zur Entfernung von Kohlendioxid (CO₂) durch Umwandlung des Moleküls in Kohlenmonoxid (CO). Anstatt Wärme zu verwenden, beruht das Verfahren im Nanobereich auf der Energie von Oberflächenplasmonen (violetter Farbton), die angeregt werden, wenn ein Elektronenstrahl (vertikaler Strahl) auf Aluminium-Nanopartikel trifft, die auf Graphit, einer kristallinen Form von Kohlenstoff, ruhen. In Gegenwart des Graphits, unterstützt durch die von den Plasmonen abgeleitete Energie, werden Kohlendioxidmoleküle (schwarzer Punkt, der an zwei rote Punkte gebunden ist) in Kohlenmonoxid (schwarzer Punkt, der an einen roten Punkt gebunden ist) umgewandelt. Das Loch unter der violetten Kugel repräsentiert das während der chemischen Reaktion weggeätzte Graphit CO₂ + C = 2CO.
NIST
Obwohl die Forscher diese Methode in einer kleinen, hochgradig kontrollierten Umgebung mit Abmessungen von nur Nanometern (Milliardstel Metern) demonstrierten, haben sie bereits Konzepte für die Skalierung der Methode und ihre praktische Anwendung in der Praxis ausgearbeitet.
Das von den Wissenschaftlern angewandte chemische Verfahren bietet nicht nur eine potenzielle neue Möglichkeit, die Auswirkungen des Klimawandels abzuschwächen, sondern könnte auch die Kosten und den Energiebedarf für die Herstellung von flüssigen Kohlenwasserstoffen und anderen von der Industrie verwendeten Chemikalien senken. Denn zu den Nebenprodukten des Verfahrens gehören die Bausteine für die Synthese von Methan, Ethanol und anderen Verbindungen auf Kohlenstoffbasis, die in der industriellen Verarbeitung verwendet werden.
Das Team zapfte eine neuartige Energiequelle aus der Nanowelt an, um eine alltägliche chemische Reaktion auszulösen, die Kohlendioxid eliminiert. Bei dieser Reaktion heftet sich fester Kohlenstoff an eines der Sauerstoffatome im Kohlendioxidgas und reduziert es zu Kohlenmonoxid. Die Umwandlung erfordert normalerweise erhebliche Energiemengen in Form von großer Hitze - eine Temperatur von mindestens 700 Grad Celsius, heiß genug, um Aluminium bei normalem atmosphärischen Druck zu schmelzen.
Anstelle von Wärme stützte sich das Team auf die Energie, die von wandernden Elektronenwellen, so genannten lokalisierten Oberflächenplasmonen (Localized Surface Plasmons, LSPs), die auf einzelnen Aluminium-Nanopartikeln surfen, gewonnen wird. Das Team löste die LSP-Oszillationen aus, indem es die Nanopartikel mit einem Elektronenstrahl anregte, der einen einstellbaren Durchmesser hatte. Ein schmaler Strahl mit einem Durchmesser von etwa einem Nanometer bombardierte einzelne Aluminium-Nanopartikel, während ein etwa tausendmal breiterer Strahl LSPs aus einer grossen Menge von Nanopartikeln erzeugte.
Im Experiment des Teams wurden die Aluminium-Nanopartikel auf einer Schicht Graphit, einer Form von Kohlenstoff, abgeschieden. Dies ermöglichte es den Nanopartikeln, die LSP-Energie auf den Graphit zu übertragen. In Gegenwart von Kohlendioxidgas, das das Team in das System injizierte, diente der Graphit dazu, einzelne Sauerstoffatome aus dem Kohlendioxid herauszuziehen und es zu Kohlenmonoxid zu reduzieren. Die Aluminium-Nanopartikel wurden bei Raumtemperatur aufbewahrt. Auf diese Weise gelang dem Team eine große Leistung: das Kohlendioxid ohne die Notwendigkeit einer hohen Wärmequelle loszuwerden.
Bisherige Methoden zur Entfernung von Kohlendioxid hatten nur begrenzten Erfolg, weil die Techniken hohe Temperaturen oder Druck erforderten, teure Edelmetalle verwendeten oder einen schlechten Wirkungsgrad hatten. Im Gegensatz dazu spart die LSP-Methode nicht nur Energie, sondern verwendet auch Aluminium, ein billiges und reichlich vorhandenes Metall.
Obwohl bei der LSP-Reaktion ein giftiges Gas - Kohlenmonoxid - erzeugt wird, verbindet sich das Gas leicht mit Wasserstoff, um essentielle Kohlenwasserstoffverbindungen wie Methan und Ethanol zu erzeugen, die häufig in der Industrie verwendet werden, sagte der NIST-Forscher Renu Sharma.
Sie und ihre Kollegen, darunter Wissenschaftler von der University of Maryland in College Park und von DENSsolutions in Delft, Niederlande, berichteten in Nature Materialsüber ihre Ergebnisse .
"Wir haben zum ersten Mal gezeigt, dass diese Kohlendioxidreaktion, die sonst nur bei 700 Grad C oder höher stattfindet, mit Hilfe von LSPs bei Raumtemperatur ausgelöst werden kann", sagte die Forscherin Canhui Wang vom NIST und der University of Maryland.
Die Forscher wählten einen Elektronenstrahl, um die LSPs anzuregen, weil der Strahl auch zur Abbildung von Strukturen im System verwendet werden kann, die nur wenige Milliardstel Meter klein sind. Auf diese Weise konnte das Team abschätzen, wie viel Kohlendioxid entfernt worden war. Sie untersuchten das System mit einem Transmissionselektronenmikroskop (TEM).
Da sowohl die Konzentration des Kohlendioxids als auch das Reaktionsvolumen des Experiments so gering waren, musste das Team spezielle Maßnahmen ergreifen, um die Menge des erzeugten Kohlenmonoxids direkt zu messen. Dazu koppelten sie einen speziell modifizierten Gaszellenhalter aus dem TEM an ein Gaschromatographen-Massenspektrometer, so dass das Team die Kohlendioxidkonzentration in Teilen pro Million messen konnte.
Sharma und ihre Kollegen verwendeten die durch den Elektronenstrahl erzeugten Bilder auch, um die Menge an Graphit zu messen, die während des Experiments weggeätzt wurde, ein Proxy dafür, wie viel Kohlendioxid entfernt worden war. Sie stellten fest, dass das Verhältnis von Kohlenmonoxid zu Kohlendioxid, das am Ausgang des Gaszellenhalters gemessen wurde, linear mit der durch das Ätzen entfernten Kohlenstoffmenge anstieg.
Die Bildgebung mit dem Elektronenstrahl bestätigte auch, dass der größte Teil des Kohlenstoffätzens - ein Proxy für die Kohlendioxid-Reduktion - in der Nähe der Aluminium-Nanopartikel stattfand. Zusätzliche Studien zeigten, dass bei Abwesenheit der Aluminium-Nanopartikel im Experiment nur etwa ein Siebtel so viel Kohlenstoff geätzt wurde.
Begrenzt durch die Grösse des Elektronenstrahls war das experimentelle System des Teams klein, nur etwa 15 bis 20 Nanometer Durchmesser (die Grösse eines kleinen Virus).
Um das System so zu vergrößern, dass es Kohlendioxid aus den Abgasen eines kommerziellen Kraftwerks entfernen kann, könnte ein Lichtstrahl eine bessere Wahl als ein Elektronenstrahl sein, um die LSPs anzuregen, sagte Wang. Sharma schlägt vor, dass eine transparente Hülle, die lose gepackte Kohlenstoff- und Aluminium-Nanopartikel enthält, über dem Schornstein eines Kraftwerks angebracht werden könnte. Eine Anordnung von Lichtstrahlen, die auf das Gitter treffen, würde die LSPs aktivieren. Wenn die Abgase durch die Vorrichtung geleitet werden, würden die lichtaktivierten LSPs in den Nanopartikeln die Energie liefern, um Kohlendioxid zu entfernen.
Die Aluminium-Nanopartikel, die im Handel erhältlich sind, sollten gleichmäßig verteilt werden, um den Kontakt mit der Kohlenstoffquelle und dem einströmenden Kohlendioxid zu maximieren, stellte das Team fest.
Die neue Arbeit deutet auch darauf hin, dass LSPs eine Möglichkeit für eine Reihe anderer chemischer Reaktionen bieten, die jetzt eine große Infusion von Energie benötigen, um bei gewöhnlichen Temperaturen und Drücken unter Verwendung von plasmonischen Nanopartikeln ablaufen zu können.
"Die Kohlendioxid-Reduktion ist eine große Sache, aber es wäre eine noch größere Sache, die enorme Energiemengen einspart, wenn wir damit beginnen könnten, viele chemische Reaktionen bei Raumtemperatur durchzuführen, die jetzt eine Erwärmung erfordern", sagte Sharma.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.

































































