Studie enthüllt neue Methode zur Herstellung von Kontrastmitteln
Dr. Benjamin Rotstein und seine Mitarbeiter stellen ein einfaches Verfahren zur Herstellung von mit Kohlenstoffisotopen markierten Medikamenten und Diagnostika vor
Dr. Benjamin Rotstein und seine Mitarbeiter stellen ein einfaches Verfahren zur Herstellung von mit Kohlenstoffisotopen markierten Arzneimitteln und Diagnostika vor.

Dr. Benjamin Rotstein, außerordentlicher Professor an der medizinischen Fakultät der Universität Ottawa, Abteilung für Biochemie, Mikrobiologie und Immunologie.
Faculty of Medicine, University of Ottawa
Die Entwicklung neuer Arzneimittel hängt von der Fähigkeit der Wissenschaftler ab, elegante und spezifische Medikamente für gezielte klinische Versuche zu entwickeln. Die Isotopenmarkierung von Arzneimittelkandidaten in den Forschungslabors ist für diese Bemühungen von entscheidender Bedeutung.
In einer neuen Studie hat das Labor von Dr. Benjamin Rotstein an der medizinischen Fakultät der Universität von Ottawa zusammen mit Kollegen eine einfache Methode zur Herstellung von mit Kohlenstoffisotopen markierten Medikamenten und Diagnostika entwickelt. Sie entwickelten eine Methode, um ein einzelnes Atom in Aminosäuren - Bausteine von Proteinen, die auch zur Herstellung von Molekülen verwendet werden - gegen sein Isotop auszutauschen.
"Dies ist für die Entwicklung von Arzneimitteln sehr wichtig, denn wir wollen wissen, wo das Medikament im Körper hingeht, wie es verstoffwechselt und ausgeschieden wird, damit wir geeignete Dosierungs- und Toxizitätsstudien planen können", sagt Dr. Rotstein, ein außerordentlicher Professor in der Abteilung für Biochemie, Mikrobiologie und Immunologie der Medizinischen Fakultät.
Die Arbeit wurde in Nature Chemistry beschrieben, einer hochrangigen Fachzeitschrift, die auch einen separaten Artikel über die Studie veröffentlichte, in dem zwei dänische Wissenschaftler der Universität Aarhus die Methoden des Teams als "wichtig für das Feld" bezeichneten.
Das Labor von Dr. Rotstein hat seine Experimente zunächst so konzipiert, dass sie wie ein Katalysator funktionieren, den unser Körper verwendet: Pyridoxalphosphat, das die Carbonsäure aus Aminosäuren entfernt und die aktive Form von Vitamin B-6 ist. Aber er sagt, dass sie es umgekehrt machen wollten, und es stellte sich heraus, dass der Mechanismus ein wenig anders war, als sie ursprünglich erwartet hatten.
"Wir fügen tatsächlich Kohlendioxid hinzu und entfernen dann die Säure. Es ist also ein anderer Mechanismus, der es uns ermöglicht, noch bessere Katalysatoren in Betracht zu ziehen und den Anwendungsbereich über Aminosäuren hinaus zu erweitern", sagt er.
Die Forschungsarbeiten wurden in Zusammenarbeit mit Kollegen der University of Alberta und Chemikern des französischen Pharmaunternehmens Sanofi durchgeführt. Das Labor von Dr. Rotstein führte die Kohlenstoff-11-Studien durch und arbeitete mit diesen Mitarbeitern zusammen, um den Mechanismus der Reaktion aufzuklären. Sein Labor verwendet Kohlenstoff-11, weil es auf eine Weise radioaktiv ist, die sich gut für die medizinische Bildgebung eignet.
Was sind die nächsten Schritte für sein uOttawa-Labor? Dr. Rotstein und sein Team untersuchen nun, wie man die Reaktion dazu bringen kann, nur eine "spiegelbildliche" Version der Aminosäuren zu produzieren, damit die Forscher sie nicht nachträglich trennen müssen.
Er sagt, dass sie besonders daran interessiert sind, Kohlenstoff-11-Aminosäuren zu verwenden, um die Geschwindigkeit zu messen, mit der unser Körper Proteine produziert, da dies ein Indikator für Krankheiten sein kann.
"Wir setzen sie auch in bildgebenden Studien ein, um mehr über den Stoffwechsel und die Proteinsyntheseraten in verschiedenen Geweben zu erfahren", sagt Dr. Rotstein, der auch Leiter des Labors für molekulare Bildgebungssonden und Radiochemie am Herzinstitut der Universität Ottawa ist.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
"Aldehyde-catalysed carboxylate exchange in α-amino acids with isotopically labelled CO2"; Nature Chemistry, 2022.
Meistgelesene News
Originalveröffentlichung
"Aldehyde-catalysed carboxylate exchange in α-amino acids with isotopically labelled CO2"; Nature Chemistry, 2022.
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
BASF erhöht Preise für Propionsäure
Hillenbrand erwirbt Coperion - Coperion ist ideale Ergänzung für amerikanisches Industrieunternehmen
Ostchemie: Tarifangleichung in Sicht
Wilhelm_Keim

AlpHa Measurement Solutions - Houston, USA
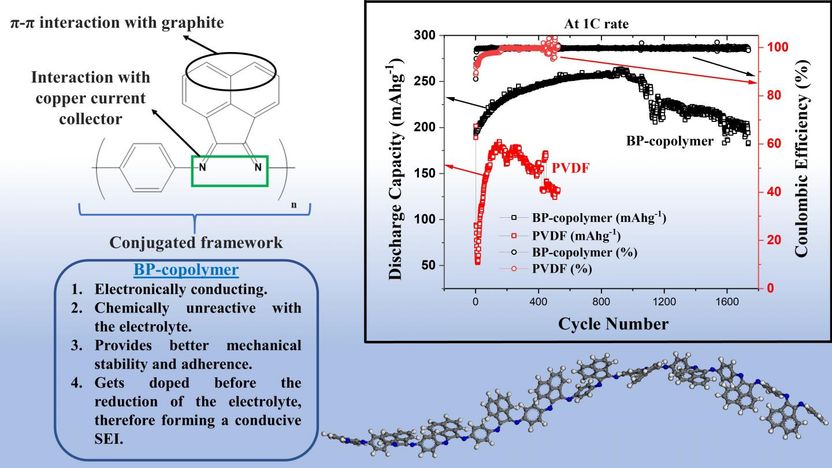
Gebaut für die Ewigkeit: Neuer Copolymer-Binder zur Verlängerung der Lebensdauer von Lithium-Ionen-Batterien - Wissenschaftler entwickeln ein neuartiges Bindermaterial, das die Graphitanode von Li-Ionen-Batterien auch nach 1700 Zyklen vor Degradation schützt

Diacolorchem EU, S.A. - Barcelona, Spanien