Proteine: Neue Materialklasse entdeckt
Wissenschaftler des Helmholtz-Zentrum Berlin (HZB) haben in Zusammenarbeit mit Forschern der chinesischen Fudan-Universität eine neue Materialklasse charakterisiert: so genannte Protein Crystalline Frameworks (PCFs).
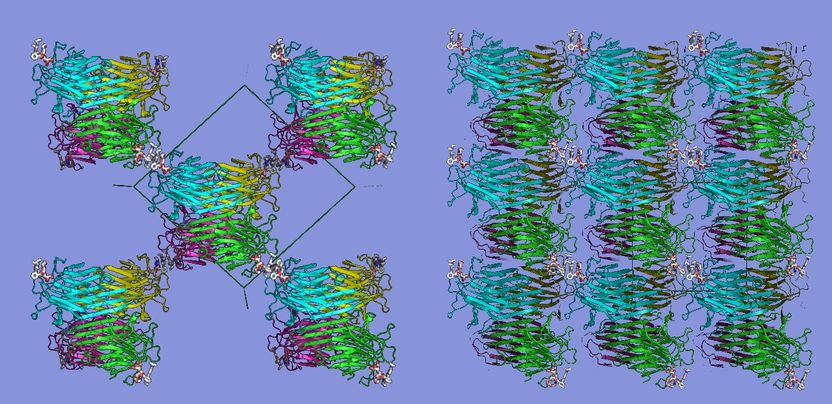
Anordnung der Concanavalin A –Proteinmoleküle in zwei verschiedenen Protein Crystalline Frameworks.
Fudan University/HZB
In den PCFs sind Proteine über bestimmte Hilfssubstanzen derart fixiert, dass sie sich symmetrisch ausrichten und sehr stabile Kristalle bilden. Die Forscher von HZB und Fudan-Universität wollen jetzt die Anwendungsmöglichkeiten der PCFs als funktionale Materialien ausloten. Ihre Ergebnisse veröffentlichen sie im Fachjournal „Nature Communications“
Jeder kennt das Phänomen vom Frühstücksei: Proteine sind empfindliche Moleküle. Unter bestimmten Umständen – etwa in kochendem Wasser – denaturieren sie, verlieren ihre natürliche Gestalt und werden fest. Zwar sind Forscher schon seit geraumer Zeit in der Lage, mit diesen Substanzen umzugehen und sie sogar so zu behandeln, dass sie Kristalle bilden. Dies gelingt aber nur unter enormem Aufwand, der sich nur für Forschungszwecke lohnt. Zudem sind auch die Protein-Kristalle sehr empfindlich.
Den Wissenschaftlern von der Fudan-Universität ist es nun erstmalig gelungen, diese Nachteile zu umgehen: Sie verknüpften das Protein Concanavalin A mit Hilfsmolekülen aus der Substanzklasse der Zucker sowie mit dem Farbstoff Rhodamin. Die so fixierten Concanavalin-Moleküle ordneten sich in dem Rahmen aus Hilfsstoffen symmetrisch an: Sie bildeten einen Kristall, in dem die Proteine stabil ineinander verschachtelt sind – ein Protein Crystalline Framework.
Die Entwicklung solch eines Molekülkonstrukts nützt nichts, wenn man nicht weiß, wie er sich bildet und wie sein Aufbau auf Ebene der Atome aussieht. Bei der Suche nach passenden Untersuchungsmöglichkeiten wandten sich die Forscher aus Shanghai an eine chinesische Wissenschaftlerin, die am HZB arbeitet. Sie wies ihre Kollegen auf die MX-Beamlines am Elektronenspeicherring BESSY II des HZB hin.
„Wir konnten am HZB mit unseren speziellen Kristallografie-Messplätzen optimale Voraussetzungen bieten, um die PCFs hochaufgelöst zu charakterisieren“, sagt Dr. Manfred Weiss, einer der leitenden Wissenschaftler des MX-Labors am HZB. Dabei wurde klar, dass man über die Hilfsmoleküle sogar steuern kann, wie stark sich die Protein-Netzwerke durchdringen. „Das gibt den PCFs eine enorme Flexibilität und Variabilität, die wir bei den nun anstehenden Forschungen zu möglichen Anwendungen stets im Auge haben werden“, so Manfred Weiss.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

AZURA Purifier + LH 2.1 von KNAUER
Präparative Flüssigkeitschromatografie - Neue Plattform für mehr Durchsatz
Damit sparen Sie Zeit und verbessern die Reproduzierbarkeit beim Aufreinigen

Holen Sie sich die Chemie-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte

Moiré-Effekt: Wie man Materialeigenschaften verdrehen kann - 2D-Materialien haben einen Boom ausgelöst. Nun zeigt sich: Spannende Effekte treten auf, wenn man zwei solche Schichtmaterialien aufeinander stapelt und leicht verdreht
Falunrot